题目内容
13.下列关于平衡常数的说法中,正确的是( )| A. | 化学平衡常数用来定量描述化学反应的限度 | |
| B. | 利用化学平衡常数判断化学反应进行的快慢 | |
| C. | 平衡常数的大小与温度、浓度、压强、催化剂有关 | |
| D. | 对于一个化学反应达到平衡之后,若只改变一个因素使得平衡发生移动,则K值一定变化 |
分析 平衡常数的大小仅与温度有关,与浓度、压强、催化剂无关,平衡常数越大,反应进行的程度就越大,据此分析.
解答 解:A.因定量描述化学反应的限度的量有:化学平衡常数和转化率,故A正确;
B.化学平衡常数与化学反应进行的快慢无关,故B错误;
C.平衡常数的大小仅与温度有关,与浓度、压强、催化剂无关,故C错误;
D.平衡常数的大小仅与温度有关,所以只要不是改变温度使得平衡发生移动,则K值一定不变,故D错误;
故选:A.
点评 本题主要考查了平衡常数的有关知识,涉及知识点较多,试题的基础性较强.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
3.已知如图转化关系中,甲、乙均为单质,下列判断正确的是( )


| A. | 甲可能是钠 | B. | 乙可能是氢气 | ||
| C. | 丙可能是氧化铝 | D. | 丙可能是三氧化硫 |
1.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为( )
| A. | v(NH3)=0.010mol•L-1•s-1 | B. | v(O2)=0.0010mol•L-1•s-1 | ||
| C. | v(NO)=0.0010mol•L-1•s-1 | D. | v(H2O)=0.045mol•L-1•s-1 |
8.有一水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:(注:已知NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O)
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.04mol气体;
第三份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g
综合上述实验,你认为以下结论正确的是( )
第一份加入AgNO3溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.04mol气体;
第三份加足量BaCl2溶液后,得到干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g
综合上述实验,你认为以下结论正确的是( )
| A. | 加入AgNO3溶液后生成的沉淀一定是AgCl | |
| B. | 该混合液中-定含有:NH4+、CO32-、SO42-,可能含K+、Cl- | |
| C. | 该混合液中一定含有:NH4+、CO32-、SO42-、Cl-,可能含K+ | |
| D. | 该混合液中:c(K+)≥0.2mol/L c(CO32-)=0.2mol/L |
18.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | 在合成氨的反应中,增大压强有利于氨的合成 | |
| B. | H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深 | |
| C. | 新制的氯水在光照下颜色变浅 | |
| D. | 氯气可以用排饱和食盐水的方法收集(Cl2+H2O═HCl+HClO) |
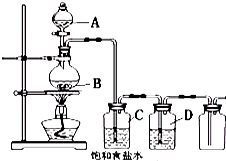 用下列装置制取并收集纯净的氯气,试回答下列问题:
用下列装置制取并收集纯净的氯气,试回答下列问题: