题目内容
11. 甲醇(CH3OH)来源丰富,价格低廉,运输储存方便,是一种重要的化工原料,有着重要的用途和应用前景.
甲醇(CH3OH)来源丰富,价格低廉,运输储存方便,是一种重要的化工原料,有着重要的用途和应用前景.(1)在25℃、101KPa下,1g甲醇(液态)燃烧生成CO2和液态水放热22.68kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol.(△H的数值保留小数点后1位)
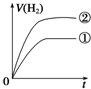
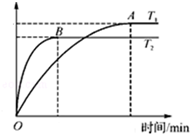
(2)工业上用CO与H2反应生成甲醇(催化剂为Cu2O/ZnO).一定条件下,在体积为3L的密闭容器中进行反应:CO(g)+2H2(g)?CH3OH(g).甲醇的物质的量随温度的变化如图所示,请回答下列问题:
①该反应正向为放热反应(填“放热”或“吸热”),升高温度,平衡常数K<(填“增大”、“减小”或“不变”).
②该反应的△S<0(填“>”或“<”)在较低(填“较高”或“较低”)温度下有利于该反应自发进行.
③温度为T2时,从反应开始到平衡,H2表示的平均反应速率v(H2)=$\frac{2nB}{3tB}$mol/(L.min).
④在其他条件不变的情况下,将处于C点的平衡体系体积压缩到原来的1/2,重新平衡时,下列有关该体系的说法正确的是BC.
A. H2的浓度减小 B.甲醇的百分含量增大 C.$\frac{c(C{H}_{3}OH)}{{c}^{2}({H}_{2})•c(CO)}$减小 D.$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大
(3)已知反应2CH3OH(g)═CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L,该时间内反应速率v(CH3OH)=0.16mol/L.
分析 (1)依据燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,题干所给量计算32g甲醇燃烧生成二氧化碳和液态水放热,结合热化学方程式书写方法,标注物质聚集状态和对应焓变;
(2)①依据图象分析温度越高平衡逆向进行,反应是放热反应分析;
②根据反应前后气体的系数和的变化确定熵变符号,根据自发性进行的盘踞:△H-T△S进行判断;
③从反应开始到平衡,在tB时间段内甲醇增加物质的量为nB,依据化学方程式计算消耗氢气物质的量为2nB,结合速率概念计算得到;
④依据平衡可知2H2+CO=CH3OH,体积压缩压强增大,分析判断选项;
(3)①K=生成物浓度幂之积与反应物浓度幂之积的比,结合平衡浓度计算,依据浓度商和平衡常数比较判断反应进行的方向;
②根据平衡常数计算平衡浓度,结合反应速率之比等于化学计量数之比计算v(CH3OH).
解答 解:(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ.32g甲醇燃烧生成二氧化碳和液态水放出热量为725.76KJ;则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ•mol-1,
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-725.76kJ•mol-1;
(2)①图象分析温度越高,甲醇物质的量减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应,升高温度平衡逆向进行,K值减小,
故答案为:放热;减小;
②反应后气体的系数和是减小的,所以熵变小于零,即△S<0,根据自发性进行的判据:△H-T△S,该放热反应△H<0,△S<0,所以在较低温度下自发进行,
故答案为:<;较低;
③反应开始到平衡,在tB时间段内甲醇增加物质的量为nB,依据化学方程式计算消耗氢气物质的量为2nB,氢气的反应速率=$\frac{2{n}_{B}}{3L{t}_{B}}$=$\frac{2nB}{3tB}$mol/(L.min);
故答案为:$\frac{2nB}{3tB}$mol/(L.min);
④其他条件不变的情况下,将处于E点的体系的体积压缩到原来的$\frac{1}{2}$,压强增大,平衡正向进行;
A.平衡正向进行,氢气物质的量减小,但体积减小为用原来的一半,氢气的浓度增大,故A错误;
B.压缩体积,增大压强,正反应速率加快,逆反应速率也加快,故B正确;
C.平衡正向进行,甲醇的物质的量增大,故C正确;
D.平衡正向进行,重新平衡时n(H2)/n(CH3OH)减小,故D错误;
故答案为:BC;
(3)①该反应的平衡常数表达式为:K=$\frac{c(C{H}_{3}OC{H}_{3})•c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$,将所给浓度带入平衡常数表达式:$\frac{0.6×0.6}{0.4{4}^{2}}$=1.86<400,故反应向正反应方向进行,正反应速率大于逆反应速率,故答案为:>;
②2CH3OH(g)≒CH3OCH3(g)+H2O(g)
某时刻浓度(mol•L-1):0.44 0.6 0.6
转化浓度(mol•L-1):2x x x
平衡浓度(mol•L-1):0.44-2x 0.6+x 0.6+x
K=$\frac{(0.6+x)^{2}}{(0.44-2x)^{2}}$,解得x=0.2mol/L,
故平衡时c(CH3OH)=0.44mol/L-0.2mol/L×2=0.04mol/L,
起始时在密闭容器中加入CH3OH,
则起始时甲醇的浓度为0.44moL/L+0.6mol/L×2=1.64mol/L,平衡时c(CH3OH)=0.04mol/L,
则10min转化甲醇1.64moL/L-0.04moL/L=1.6mol/L,
所以甲醇的反应速率为v(CH3OH)=$\frac{1.6mol/L}{10min}$=0.16 mol/(L•min),
故答案为:0.04 mol•L-1; 0.16 mol/(L•min).
点评 本题考查热化学方程式的书写、反应速率的计算、图象分析判断反应特征,平衡影响因素的分析理解,掌握基础是解题关键,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 0.3 mol•L-1 | B. | 0.4 mol•L-1 | C. | 0.5 mol•L-1 | D. | 0.6 mol•L-1 |
| A. | 0.2Q | B. | 0.1Q | C. | 5Q | D. | 10Q |
| A. | 浓硝酸存放在带橡胶塞的棕色玻璃瓶中 | |
| B. | 四氯化碳萃取溴水中的溴时,水从分液漏斗下口流出 | |
| C. | 向饱和的NaCl溶液中通入足量的NH3后,再通入CO2,有晶体析出 | |
| D. | 某溶液中滴加BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液中一定含有Ag+ |

| A. | 甲可能是钠 | B. | 乙可能是氢气 | ||
| C. | 丙可能是氧化铝 | D. | 丙可能是三氧化硫 |
| A. | v(NH3)=0.010mol•L-1•s-1 | B. | v(O2)=0.0010mol•L-1•s-1 | ||
| C. | v(NO)=0.0010mol•L-1•s-1 | D. | v(H2O)=0.045mol•L-1•s-1 |