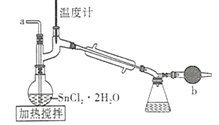
МвДїДЪИЭ
ЎѕМвДїЎїЈЁ1Ј©Мъј°МъµД»ЇєПОпУ¦УГ№г·єЈ¬ИзFeCl3їЙУГЧчґЯ»ЇјБЎўУЎЛўµзВ·Н°еёЇКґјБєННвЙЛЦ№СЄјБµИЎЈРґіцFeCl3ИЬТєёЇКґУЎЛўµзВ·Н°еµДАлЧУ·ЅіМКЅ___ЎЈёЇКґН°еєуµД»мєПИЬТєЦРЈ¬ИфCu2+ЎўFe3+єНFe2+µДЕЁ¶ИѕщОЄ0.10mol/LЈ¬ЗлІОХХПВ±нёшіцµДКэѕЭєНТ©Ж·Ј¬јтКціэИҐCuCl2ИЬТєЦРFe3+єНFe2+µДКµСйІЅЦи___ЎЈ
ЗвСх»ЇОпїЄКјіБµнК±µДpH | ЗвСх»ЇОпіБµнНкИ«К±µДpH | |
Fe3+ Fe2+ Cu2+ | 1.9 7.0 4.7 | 3.2 9.0 6.7 |
МṩµДТ©Ж·ЈєCl2 ЕЁH2SO4 NaOHИЬТє CuO Cu | ||
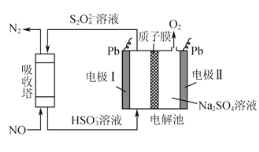
ЈЁ2Ј©јдЅУµз»ЇС§·ЁїЙ¶ФґуЖшОЫИѕОпNOЅшРРОЮє¦»Їґ¦АнЈ¬Ж乤ЧчФАнИзНјЛщКѕЈ¬ЦКЧУД¤ФКРнH+єНH2OНЁ№эЎЈµзј«ўсОЄ___ј«Ј¬µзј«·ґУ¦КЅОЄ___Ј¬ОьКХЛюЦРµД·ґУ¦ОЄ____Ј¬Гїґ¦Ан1molNOЈ¬їЙН¬К±µГµЅ___gO2ЎЈ
ЈЁ3Ј©Ў°ЦШУН-СхЖш-ИЫИЪМјЛбДЖЎ±ИјБПµзіШЧ°ЦГИзНјЛщКѕЎЈПВБРЛµ·ЁґнОуµДКЗЈЁ______Ј©
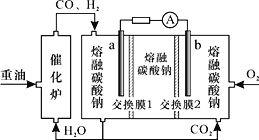
A.O2ФЪbј«µГµзЧУЈ¬ЧоЦХ±»»№ФОЄCO32-
B.·Еµз№эіМЦРЈ¬µзЧУУЙµзј«aѕµјПЯБчПтµзј«b
C.ёГµзіШ№¤ЧчК±Ј¬CO32-ѕЎ°Ѕ»»»Д¤2Ў±ТЖПтbј«
D.H2ІОУлµДµзј«·ґУ¦ОЄH2-2e-+CO32-=H2O+CO2
Ўѕґр°ёЎї2Fe3++Cu=2Fe2++Cu2+ ўЩНЁИлЧгБїВИЖшЅ«Fe2+Сх»ЇіЙFe3+Ј»ўЪјУИлCuOµчЅЪИЬТєµДpHЦБ3.2©Ѓ4.7Ј»ўЫ№эВЛЈЁіэИҐFeЈЁOHЈ©3Ј© Тх 2HSO3-+2e-+2H+ЁTS2O42-+2H2O 2NO+2S2O42-++2H2O=N2+4HSO3- 16 C
ЎѕЅвОцЎї
(1)Fe3+УРЗїСх»ЇРФЈ¬ДЬ°СЅрКфНСх»ЇіЙНАлЧУЈ»ПИЅ«Fe2+ЧЄ»ЇіЙFe3+Ј»ФЩёщѕЭНј±нМхјюИЬТєµДpHЦµЈ¬ИэјЫМъАлЧУіБµнНкИ«єуЈ¬ЅшРР№эВЛјґїЙЈ»
(2)µзј«IОЄТхј«Ј¬Фтµзј«ўтОЄСфј«Ј¬µзЅвіШЦРСфАлЧУПтТхј«ТЖ¶ЇЈ¬HSO3-ФЪµзј«IЙПЧЄ»ЇОґS2O42-Ј¬№эіМЦРSµД»ЇєПјЫЅµµНЈ¬µГµЅµзЧУ·ўЙъ»№Ф·ґУ¦Ј¬Фтµзј«IОЄТхј«Ј»ОьКХЛюЦРНЁИлNOєНS2O42-АлЧУ·ґУ¦Ј¬ЙъіЙN2єНHSO3-Ј¬ѕЭґЛРґіц·ґУ¦·ЅіМКЅЈ»ґ¦АнNOК±Ј¬ІъЙъHSO3-ЅшИлµзЅвіШЈ¬O2ТЭіцµзЅвіШЈ¬S2O42-БчіцµзЅвіШЈ¬ѕЭґЛјЖЛгµзЅвіШµДЦКБї±д»ЇЈ»
(3)ИјБПµзіШНЁO2µДј«ОЄХэј«Ј¬·ўЙъ»№Ф·ґУ¦Ј¬ИјБПФЪёєј«·ўЙъСх»Ї·ґУ¦Ј»ФµзіШ№¤ЧчК±µзЧУСШµјПЯБчПтХэј«Ј¬µзіШДЪІїТхАлЧУПтёєј«ТЖ¶ЇЎЈ
(1)Fe3+УРЗїСх»ЇРФЈ¬ДЬ°СЅрКфНСх»ЇіЙНАлЧУЈ¬ЧФЙн±»»№ФіЙ Fe2+Ј¬·ґУ¦·ЅіМКЅОЄ2Fe3++Cu=2Fe2++Cu2+Ј»ёщѕЭНј±нЦЄЈ¬Fe3+іБµнРиТЄµДPHЦµЅПРЎЈ¬УлНАлЧУіБµнК±µДPHЦµПаІоЅПґуЈ¬ЛщТФКЧПИЅ«¶юјЫМъАлЧУЧЄ»ЇОЄИэјЫМъАлЧУЈ¬СЎИЎµДКФјБІ»ДЬТэЅшРВµДФУЦКАлЧУЈ¬ЛщТФСЎИЎВИЖш ЧчСх»ЇјБЈ»И»єујУИИСх»ЇНіэИҐВИЖшИЬЅвЙъіЙµДСОЛбЈ¬ФЪPHЦµ3.2К±ИэјЫМъАлЧУНкИ«іБµнЈ¬PHЦµ4.7К±НАлЧУїЄКјіБµнЈ¬ЛщТФµчЅЪИЬТєµДPHЦµЦБ3.2-4.7Ј»И»єуНЁ№э№эВЛіэИҐЙъіЙµДіБµнЈ»
(2)HSO3-ФЪµзј«IЙПЧЄ»ЇОґS2O42-Ј¬№эіМЦРSµД»ЇєПјЫЅµµНЈ¬µГµЅµзЧУ·ўЙъ»№Ф·ґУ¦Ј¬Фтµзј«IОЄТхј«Ј¬µзј«·ґУ¦ОЄЈє2HSO3-+2e-+2H+ЁTS2O42-+2H2OЈ»ОьКХЛюЦРНЁИлNOєНS2O42-АлЧУ·ґУ¦Ј¬ЙъіЙN2єНHSO3-Ј¬ЛщТФ·ґУ¦·ЅіМКЅОЄЈє2NO+2S2O42-+2H2O=N2+4HSO3-Ј»µзј«ўтОЄСфј«Ј¬H2OФЪµзј«ўтЙП±»ЧЄ»ЇОЄO2Ј¬·ўЙъµзј«·ґУ¦Јє2H2O-4e-ЁTO2Ўь+4H+Ј¬Гїґ¦Ан1molNOЈ¬ФтЧЄТЖµзЧУКэОЄ1molЎБ2=2molЈ¬ёщѕЭµзЧУЧЄТЖКШєгЈ¬ФтІъЙъO2µДОпЦКµДБїОЄ2molЎБ![]() =0.5molЈ¬ЦКБїОЄ0.5molЎБ32g/mol=16gЈ»
=0.5molЈ¬ЦКБїОЄ0.5molЎБ32g/mol=16gЈ»
(3)AЈ®СхЖшТ»ј«ОЄХэј«Ј¬·ўЙъ»№Ф·ґУ¦Ј¬ЛщТФO2ФЪbј«µГµзЧУЈ¬ЧоЦХ±»»№ФОЄCO32-Ј¬№КAХэИ·Ј»
BЈ®ФµзіШЦРµзЧУСШµјПЯБчПтХэј«Ј¬ЛщТФ·Еµз№эіМЦРЈ¬µзЧУУЙµзј«aѕµјПЯБчПтµзј«bЈ¬№КBХэИ·Ј»
CЈ®ФµзіШЦРТхАлЧУПтёєј«ТЖ¶ЇЈ¬ЛщТФCO32-ѕЎ°Ѕ»»»Д¤2Ў±ТЖПтaј«Ј¬№КCґнОуЈ»
DЈ®ёєј«ЗвЖш·ўЙъСх»Ї·ґУ¦Ј¬µзј«·ґУ¦КЅЈєH2-2e-+CO32-ЁTH2O+CO2Ј¬№КDХэИ·Ј»
№Кґр°ёОЄCЎЈ

 С§Б·їміµµАїмАЦјЩЖЪє®јЩЧчТµПµБРґр°ё
С§Б·їміµµАїмАЦјЩЖЪє®јЩЧчТµПµБРґр°ё РВЛјО¬є®јЩЧчТµПµБРґр°ё
РВЛјО¬є®јЩЧчТµПµБРґр°ёЎѕМвДїЎїИзНјКЗДіјУµвКіСО°ьЧ°ґьЙПµДІї·ЦНј±нОДЧЦ(IОЄµвФЄЛШ·ыєЕ)ЎЈУЙґЛЈ¬ДгµГµЅµДРЕПўєНЧчіцµДНЖІвКЗ( )

ВИ»ЇДЖ (NaCl) | ЎЭ98.0% (ТФNaClјЖ) |
µвЛбјШ (KIO3) | (35ЎА15)mg/kg (ТФIјЖ) |
A.ґЛКіСОКЗґїѕ»Оп
B.Ў°јУµвКіСОЎ±ЦРµДЎ°µвЎ±КЗЦёµҐЦК
C.1kgґЛКіСОЦРє¬µвЛбјШ(35ЎА15)mg
D.ІЛОґЙХКмІ»ТЛјУИлјУµвµДФТтїЙДЬКЗµвЛбјШКЬИИІ»ОИ¶Ё
ЎѕМвДїЎїПВБРёчЧйОпЦКЦРЈ¬ОпЦКЦ®јдНЁ№эТ»ІЅ·ґУ¦ѕНДЬКµПЦИзНјЛщКѕЧЄ»ЇµДКЗЈЁЎЎЎЎЈ©
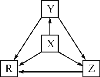
СЎПо | X | Y | Z | R |
A | Al | AlCl3 | Al(OH)3 | NaAlO2 |
B | Na | Na2O | Na2O2 | NaOH |
C | H2S | S | SO2 | SO3 |
D | N2 | NH3 | NO | NO2 |
A.AB.BC.CD.D
ЎѕМвДїЎїОВ¶ИОЄTК±Ј¬Пт2.0LєгИЭГЬ±ХИЭЖчЦРідИл1.0mol PCl5Ј¬·ґУ¦PCl5ЈЁgЈ©PCl3ЈЁgЈ©+Cl2ЈЁgЈ©,ѕ№эТ»¶ОК±јдєуґпµЅЖЅєвЎЈ·ґУ¦№эіМЦРІв¶ЁµДІї·ЦКэѕЭјыПВ±нЈє
t/s | 0 | 50 | 150 | 250 | 350 |
nЈЁPCl3Ј©/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
ПВБРЛµ·ЁХэИ·µДКЗЈЁЎЎЎЎЈ©
A.·ґУ¦ФЪ50sК±µДЛЩВКvЈЁPCl3Ј©ЈЅ0.0016molL©Ѓ1s©Ѓ1
B.±ЈіЦЖдЛыМхјюІ»±дЈ¬ЙэёЯОВ¶ИЈ¬ЖЅєвК±cЈЁPCl3Ј©ЈЅ0.11molL©Ѓ1Ј¬Фт·ґУ¦µДЎчHЈј0
C.ПаН¬ОВ¶ИПВЈ¬ЖрКјК±ПтИЭЖчЦРідИл1.0molPCl5Ўў0.20molPCl3єН0.20molCl2Ј¬·ґУ¦ґпµЅЖЅєвЗ°vЈЁХэЈ©ЈѕvЈЁДжЈ©
D.ПаН¬ОВ¶ИПВЈ¬ЖрКјК±ПтИЭЖчЦРідИл2.0molPCl3єН2.0molCl2Ј¬ґпµЅЖЅєвК±Ј¬PCl3µДЧЄ»ЇВКРЎУЪ80%