题目内容
13.下列关于元素周期律的叙述正确的是( )| A. | 随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 | |
| B. | 随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 | |
| C. | 随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 | |
| D. | 元素原子的核外电子排布、原子半径及元素主要化合价的都发生周期性变化 |
分析 A.在第一周期,随着元素原子序数的递增,原子最外层电子数总是从1到2;
B.元素的最低负价是-4价,最高正价是+7价;
C.同主族元素从上到下原子半径逐渐增大;
D.元素性质的周期性变化是由原子结构的周期性变化引起的.
解答 解:A.从第二周期开始,随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现,而在第一周期,随着元素原子序数的递增,原子最外层电子数总是从1到2,故A错误;
B.元素的最低负价是-4价,最高正价是+7价,随着元素原子序数的递增,一般情况下元素的最高正价从+1到+7,负价从-4到-1重复出现,故B错误;
C.同主族元素从上到下原子核外电子层数逐渐增多,原子半径逐渐增大,原子核外电子层数越多,半径越大,故C错误;
D.元素性质的周期性变化是由原子结构的周期性变化引起的,则原子核外电子排布、原子半径及元素主要化合价的周期性变化,故D正确.
故选D.
点评 本题考查元素周期表和元素周期律知识,为高考常见题型,侧重于基础知识的考查,能很好地培养学生的良好的科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
3.设NA为阿伏加德罗常数.下列说法错误的是( )
| A. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA | |
| B. | 常温常压下,64 g O2和O3混合气体中含有原子总数为4NA | |
| C. | 1mol Cl2与NaOH溶液反应,转移的电子总数为2NA | |
| D. | 标准状况下,22.4L N2含共用电子对数为3NA |
4.在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法正确的是( )
| A. | Na2CO3溶液:c(Na+)>c(CO32-)>c(OH-)>c(H+) | |
| B. | 升高温度,溶液pH减小 | |
| C. | 稀释溶液,溶液中所有离子浓度都减小 | |
| D. | 加入Ba(OH)2固体c(CO32-)增大 |
1.下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )
| A. | NaOH | B. | SiO2 | C. | Fe | D. | H2Se |
18.下列对合成材料的认识不正确的是( )
| A. | 有机高分子化合物称为聚合物或高聚物,是因为它们大部分是由小分子通过聚合反应而制得的 | |
| B. | 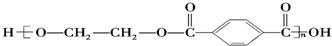 的单体是HOCH2OH与 的单体是HOCH2OH与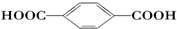 | |
| C. | 聚乙烯( )是由乙烯加聚生成的纯净物 )是由乙烯加聚生成的纯净物 | |
| D. | 高分子材料可分为天然高分子材料和合成高分子材料两大类 |
5.脑白金是热卖中的一种滋补品,其有效成分的结构简式如图.下列对该化合物的叙述正确的是 ( )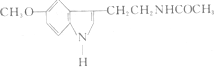

| A. | 它属于芳香烃 | B. | 它属于高分子化合物 | ||
| C. | 分子式为C13 H15N2O2 | D. | 在一定条件下可以发生加成反应 |
2.桶烯结构简式如图所示,有关说法不正确的是( )
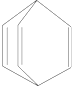

| A. | 桶烯在一定条件下能发生加聚反应 | |
| B. | 桶烯与苯乙烯(C6H5CH═CH2)互为同分异构体 | |
| C. | 桶烯中的一个氢原子被氯原子取代,所得产物只有两种 | |
| D. | 桶烯分子中所有的原子在同一平面上 |
 )的一种工业制法
)的一种工业制法 →浓盐酸Zn-HgR1-CH2-R2(其中R1、R2表示烃基或氢原子)
→浓盐酸Zn-HgR1-CH2-R2(其中R1、R2表示烃基或氢原子) +RCOOH
+RCOOH
 、G
、G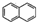 、H
、H .
. .
. (其中一种).
(其中一种).