题目内容
【题目】【2016届邯郸一模】碳铵是一种较常使用的化肥,它在常温下易分解。某化学兴趣小组对碳铵的成分存在疑问,时行了如下探究。
【定性实验】检验溶液中的阴、阳离子
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成.再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色。
(1)根据实验现象,推测碳铵中所含有阴离子可能是_______和_______;
(2)根据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是__________________;
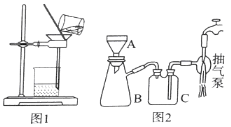
【定量试验】测定碳铵中C元素和N元素质量比.该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如图所示.
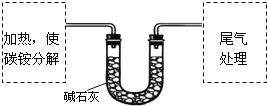
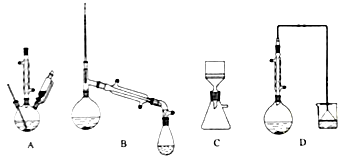
(3)碳铵固体应放在________中进行加热.
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
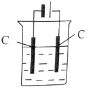
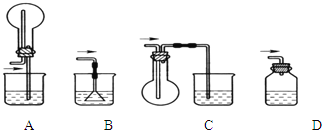
(4)从安全的角度考虑,尾气处理的装置可以选用________;
(5)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg.由此测得N元素的质量是_____g。
(6)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量.请你评价该方案是否合理;_______(填“合理”“不合理”),理由是________。
【答案】(13分)(1)HCO3-、CO32- (各1分,共2分)
(2)NH4++OH-![]() NH3↑+H2O 或NH4++HCO3-+2OH-
NH3↑+H2O 或NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O (2分)
NH3↑+CO32-+2H2O (2分)
(3)A(2分) (4)A(2分) (5)![]() (2分)
(2分)
(6)本小题属于开放性试题,若考生只回答“合理”或“不合理”不给分;若考生回答“合理”或“不合理”且理由能做出相应解释,可酌情给分(3分)。例如:考生回答
①不合理,因为碳铵中可能含有HCO3-,不能与BaCl2产生沉淀,所测得碳元素质量分数不准确。
②合理,因为碳铵中只含有CO32-,加入BaCl2能完全生成沉淀,可准确测得碳元素的质量”。
【解析】
试题分析:【定性实验】取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成,白色沉淀为碳酸钙,盐中阴离子可能HCO3-、CO32-;再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色,则气体为氨气,则原固体中含铵根离子,(1)由上述分析可知,阴离子可能为HCO3-、CO32-;
(2)碳铵与足量NaOH溶液加热反应的离子方程式可能是NH4++OH-=NH3↑+H2O、HCO3-+OH-=CO32-+H2O(或NH4++HCO3-+2OH-=NH3+CO32-+2H2O);
【定量实验】ag碳铵,加热使之分解,碱石灰增重为水和二氧化碳的质量,尾气处理为氨气,(3)因加热装置后连接U形管,则选择仪器只能为试管,故答案为A;
(4)尾气处理,应防止倒吸,B不能防止倒吸,C中气体收集时导管应短进,D中为密闭容器可能会炸裂,只有A装置收集及防倒吸,故答案为A;
(5)灼烧后没有固体残余,称量U形管在实验前后的质量差为bg,则氨气的质量为(a-b)g,则含N质量为![]() g;
g;
(6)ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量,则①不合理,因为碳铵中可能含有HCO3-不能与BaCl2产生沉淀所测得碳元素质量分数不准确;②合理,因为碳铵中只含有CO32-加入BaCl2能完全生成沉淀可准确测得碳元素的质量;③不合理;测得的结果不准确。

 备战中考寒假系列答案
备战中考寒假系列答案