题目内容
【题目】KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
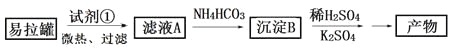
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
【答案】(1)d (2分)
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑ (2分)
(3)Al(OH)3Al3+水解,使溶液中H+浓度增大(每空1分,共2分)
(4)20 (2分)
【解析】试题分析:(1)易拉罐(主要成分为Al,含有少量的Fe、Mg杂质),它们都是比较活泼的金属,都可以与酸发生反应,而Al可以与强碱溶液反应变为NaAlO2进入溶液,而Fe、Mg不能与碱发生反应,所以要以含Al的易拉罐为原料制取明矾,应该用强碱NaOH溶液溶解,选项d正确;Mg、Fe不溶解,会留在滤渣中;(2)易拉罐溶解过程中主要反应的化学方程式为2Al+2NaOH+2H2O==2NaAlO2+3H2↑,反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑;(3)滤液A的主要成分是NaAlO2,向其水溶液中加入NH4HCO3溶液,AlO2-、NH4+发生盐的双水解反应,产生Al(OH)3沉淀和NH3·H2O,反应的方程式是AlO2-+2H2O+NH4+= Al(OH)3↓+NH3·H2O,所以沉淀B化学式为Al(OH)3;将少量明矾溶于水,溶液呈弱酸性,其原因是该盐是强酸弱碱盐,Al3+发生水解反应,消耗水电离产生的OH-,当最终达到平衡时溶液中c(H+)>c(OH-),所以溶液显酸性。(4)已知:Kw=1.0×10-14,Al(OH)3![]() AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数K=
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数K= 。
。