题目内容
【题目】A.B.C.D.E.F六种短周期元素的原子序数依次增大。已知A.C.F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
(1)写出下列元素的符号A___________,D___________,E___________;
(2)用电子式表示B、F形成的化合物___________;
(3)A、C两种元素最高价氧化物的水化物之间反应的离子方程式_____________;
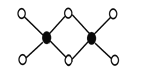
(4)D的固态氧化物是________晶体。含n mol D的氧化物的晶体中含D-O共价键为_______mol
【答案】(1)Na;Si;P
(2)![]()
(3)Al(OH)3+OH-=AlO2-+2H2O
(4)原子;4n
【解析】试题分析:A、B、C、D、E、F六种短周期元素的原子序数依次增大,D元素的最外层电子数比次外层电子数少4,D原子只能有3个电子层,原子最外层电子数为8-4=4,则D为Si元素;E元素原子次外层电子数比最外层电子数多3,E原子有3个电子层,最外层电子数为8-3=5,则E为磷元素;A、C、F三种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,则含有Al元素,氢氧化铝溶于强酸、强碱,故有Na元素,则A为Na、C为Al,三种原子最外层共有11个电子,则E的最外层电子数为11-1-3=7,则F为Cl元素,结合原子序数可知B为Mg。
(1)由上述分析可知,A为Na,D为Si,E为为P。
故答案为:Na;Si;P;
(2)B、F形成的化合物为氯化镁,用电子式表示其形成过程为![]() 。
。
故答案为:![]() ;
;
(3)A、C两种元素最高价氧化物的水化物之间反应的离子方程式为:Al(OH)3+OH-═AlO2- +2H2O。
故答案为:Al(OH)3+OH-═AlO2- +2H2O;
(4)D为Si元素,其氧化物为二氧化硅,二氧化硅属于原子晶体;Si能形成4个共价键,nmol二氧
化硅中含有nmolSi原子,所以nmol二氧化硅含4nmolSi-O键。
故答案为:原子;4n。

 智慧小复习系列答案
智慧小复习系列答案