题目内容
13.下列试剂可以鉴别BaS03中是否含有BaS04的是 ( )| A. | Ba(NO3)2溶液 | B. | 盐酸 | C. | 硫酸钠 | D. | 酚酞 |
分析 BaS03具有还原性,可被氧化生成硫酸钡,且BaS03溶于盐酸,以此解答.
解答 解:A.加入Ba(NO3)2溶液,都不反应,不能鉴别,故A错误;
B.BaS03溶于盐酸,而硫酸钡不溶,可鉴别,故B正确;
C.二者都不溶于硫酸钠溶液,不能鉴别,故C错误;
D.酚酞溶液不能鉴别二者,故D错误.
故选B.
点评 本题考查离子的鉴别,为高频考点,明确氧化还原反应的应用及萃取现象是解答本题的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案
相关题目
1.在无色的水溶液中能大量共存的一组离子是( )
| A. | Al3+、Na+、Cl-、H+ | B. | H+、Fe2+、ClO-、Cl- | ||
| C. | Na+、Al3+、Cl-、OH- | D. | K+、Ba2+、Cu2+、Cl- |
8.下列溶液在常温下pH<7的是 ( )
| A. | KCl溶液 | B. | CH3CH2OH溶液 | C. | CH3COOH溶液 | D. | NaOH溶液 |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 16g CH4含有4NA个电子 | |
| B. | 0.1mol铁和0.1mol铜分别与0.1mol氯气完全反应,转移的电子数均为0.2NA | |
| C. | 标准状况下,11.2L H2O中分子数为0.5NA个 | |
| D. | 0.1mol•L-1 Na2CO3溶液中含有0.2NA个Na+ |
5.设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A. | 6g SiO2晶体中含有0.4NA个Si-O键 | |
| B. | PH=12的Na2CO3中有0.01NA个水分子发生了电离 | |
| C. | 标况下,11.2LHF含有的HF分子数大于0.5NA | |
| D. | 把含1molFeCl3的饱和溶液滴入沸水煮沸至红褐色透明,停止加入后,小于1NA |
2.某温度时,在恒容密闭容器中,X、Y、Z三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图II所示.则下列结论正确的是( )
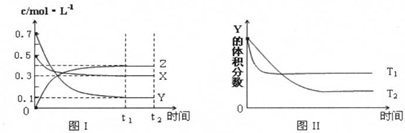

| A. | 该反应的热化学方程式为:3X(g)+Y(g)?4Z(g);△H>0 | |
| B. | 若其它条件不变,平衡后又加入一定量X,正速率增大、逆速率减小,X的转化率减小 | |
| C. | 达到平衡后,若其他条件不变,升高温度,平衡向逆反应方向移动 | |
| D. | 达到平衡后,若其他条件不变,减小容器体积,平衡不移动 |
7.实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2+H2OCH2=CH2Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据如右:
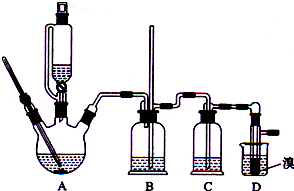
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度 c.防止乙醇挥发d.减少副产物乙醚生成
(2)反应过程中A装置可能产生的酸性干扰气体SO2(填化学式),为此在装置C中应加入c(从下列选项中选择)以吸收除杂.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.高锰酸钾溶液
(3)装置B是安全瓶,其工作原理是当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大.
(4)若产物中有少量未反应的Br2,最好用下列试剂中的c洗涤(填选项符号),再通过分液的方法分离;
a.水 b.氢氧化钠溶液 c.NaHSO3溶液 d.苯
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2+H2OCH2=CH2Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据如右:

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d;(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度 c.防止乙醇挥发d.减少副产物乙醚生成
(2)反应过程中A装置可能产生的酸性干扰气体SO2(填化学式),为此在装置C中应加入c(从下列选项中选择)以吸收除杂.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.高锰酸钾溶液
(3)装置B是安全瓶,其工作原理是当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大.
(4)若产物中有少量未反应的Br2,最好用下列试剂中的c洗涤(填选项符号),再通过分液的方法分离;
a.水 b.氢氧化钠溶液 c.NaHSO3溶液 d.苯
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去;
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.