题目内容
短周期金属元素甲-戊在元素周期表中的相对位置如表所示,下面判断正确的是( )
| 甲 | 丙 | |
| 乙 | 丁 | 戊 |
A.原子半径: 丙<丁<戊
B.金属性:丙>甲
C.最高价氧化物对应的水化物碱性:乙>丁>戊
D.戊只与强酸反应
C
解析试题分析:A.同周期原子半径从左向右在减小,则原子半径为丙>丁>戊,故A正确;B.同 主族从上到下元素的金属性在增强,则金属性为甲<丙,故B错误;C.同周期从左向右金属性减弱,金属性越强,对应的最高价氧化物的水化物的碱性越强,则氢氧化物碱性为丙>丁>戊,故C正确;D.同周期从左向右最外层电子数增大,同主族最外层电子数相同,则最外层电子数为乙=丁>甲=丙,故D正确;故选B。
考点:本题考查元素周期律和元素周期表,熟悉同主族.同周期元素性质的变化规律即可解答,题目难度不大。

练习册系列答案
相关题目
很多国家已停止使用含铊的杀虫剂。元素周期表中铊的数据见右图,下列说法正确的是
| A.TI元素是一种主族元素 |
| B.TI元素的相对原子质量是204 |
| C.铊元素的质量数是204.4 |
| D.TI原子最外层有3个能量相同的电子 |
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等,则
| A.原子半径:丙>乙>丁 |
| B.单质的还原性:丁>丙>甲 |
| C.甲、乙、丙的氧化物均为共价化合物 |
| D.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
几种短周期元素的原子半径及主要化合价如下表 ( )
| 元素代号 | X | Y | Z | M | N | P |
| 原子半径/nm | 0.186 | 0.143 | 0.075 | 0.074 | 0.152 | 0.099 |
| 元素的主要化合价 | +1 | +3 | +5、-3 | -2 | +1 | +7、-1 |
下列叙述错误的是(其中NA表示阿伏加德罗常数的值)
A.X、N元素的金属性:X>N
B.Y、M元素形成的离子化合物是工业冶炼Y的原料
C.X单质在M单质中燃烧生成的化合物39g中共含有0.5NA个阴离子
D.标准状况下1L 1mol·L-1的YP3溶液中含有NA个Y3+离子
下列叙述与对应图式正确的是
A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强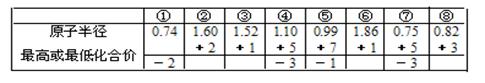 |
B.图甲表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2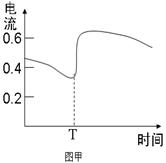  |
| C.图乙表示某一放热反应,若使用催化剂E1、E2、ΔH都会发生改变 |
| D.表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H= -571.6kJ/mol |
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是
| | Q | R | |
| T | | | W |
A.T的氧化物是光导纤维的主要成分
B.W的氢化物的化学式为HCl
C.R的最高正价氧化物的水化物是弱电解质
D.Q与氢形成的化合物均含极性共价键
下图为元素周期表中短周期的一部分,下列说法正确的是
| ① | ② | ③ |
| ④ | ⑤ | ⑥ |
A.①~⑥可能全部是非金属元素
B.对应单质的活泼性:②>③
C.④的最高价氧化物对应的水化物可能为两性物质
D.②、⑤的最高价氧化物对应的水化物可能均为强酸
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
| A.R的单质能与W的氢化物反应,可证明非金属性:R>W |
| B.最高正价氧化物对应的水化物的酸性:R<W |
| C.X与Z组成的化合物是共价化合物,且又具有两性 |
| D.离子半径:Z>Y>X |