题目内容
18.下列原因解释与氢键无关的( )| A. | CH4的沸点比SiH4低,而CH4比SiH4热稳定性强 | |
| B. | 有机物大多难溶于水,而乙醇和乙酸可与水互溶 | |
| C. | H2O2和H2S的相对分子相近,而H2O2的沸点远高于H2S | |
| D. | 采用加压液化的方法从氨合成塔里分离出NH3 |
分析 氢键是分子间作用力的一种,多物质的物理性质有显著的影响,存在氢键的物质,水溶性显著增强,分子间作用力增强,熔沸点升高,含氮、氧、氟的氢化物易形成氢键.
A.CH4、SiH4为分子晶体,熔点随相对分子质量增加而升高,非金属性越强,则对应的氢化物的稳定性越大,与氢键无关;
B.乙醇和乙酸含有羟基,能和水形成氢键;
C.氢键影响物质的沸点和溶解性,H2O2为含有氢键的物质;
D.氨气分子间能形成氢键,合成氨采用分离产物的方法促进平衡正移,提高转化率;
解答 解:A.CH4、SiH4为分子晶体,分子晶体溶沸点与分子量成正比,甲烷分子量大于硅烷,CH4的沸点比SiH4低,非金属性越强,则对应的氢化物的稳定性越大,同主族元素从上到下元素的非金属性减弱,C、Si同主族,则氢化物按稳定性由弱到强的顺序为SiH4<CH4,与氢键无关,故A正确;
B.乙醇和乙酸含有羟基,都能与水分子之间存在氢键,使甲醇的水溶性显著增强,与氢键有关,故B错误;
C.O元素非金属性较强,对应的氢化物能形成氢键,且与水分子之间也可以形成氢键,硫元素和水分子间不能形成氢键,所以H2O2的沸点比H2S高,与氢键有关,故C错误;
D.N元素非金属性较强,对应的氢化物能形成氢键,氨气分子间能形成氢键,采用加压液化的方法,促进平衡正移,提高转化率,故D错误;
故选A.
点评 本题考查了氢键对物质性质的影响,题目难度不大,注意氢键的存在只影响物质的物理性质,与物质的化学性质无关.

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
1. 下表是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:
下表是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:
(1)在元素 ①~⑧中,非金属性最强的元素是F(填元素符合).
(2)在元素 ①~⑧中,原子半径最大的是钠(填元素名称).
(3)元素⑤⑥⑦的最高价氧化物对应水化物,按碱性从强到弱的排列顺序是NaOH>Mg(OH)2>Al(OH)3(用化学式表示).
(4)用电子式表示元素①和⑧组成的化合物的形成过程 .
.
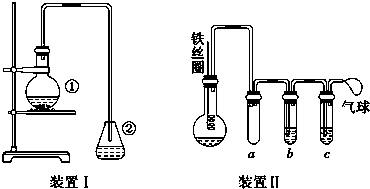
(5)为验证VIIA族部分元素非金属性的递变规律,设计了如图装置进行实验,请回答:
①仪器A的名称是分液漏斗,A中发生的反应的离子方程式是2Br-+Cl2=Br2+2Cl-.
②棉花中浸有的NaOH溶液的作用是(用离子方程式表示)Cl2+2OH-=Cl-+ClO-+H2O.
③为验证溴与碘非金属性强弱:通入少量⑧的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到溶液分层,上层几乎无色,下层呈紫红色.
④VIIA族元素,非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下,电子层数增多,原子半径逐渐增大,得电子能力逐渐减弱.
 下表是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:
下表是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)在元素 ①~⑧中,原子半径最大的是钠(填元素名称).
(3)元素⑤⑥⑦的最高价氧化物对应水化物,按碱性从强到弱的排列顺序是NaOH>Mg(OH)2>Al(OH)3(用化学式表示).
(4)用电子式表示元素①和⑧组成的化合物的形成过程
 .
.(5)为验证VIIA族部分元素非金属性的递变规律,设计了如图装置进行实验,请回答:
①仪器A的名称是分液漏斗,A中发生的反应的离子方程式是2Br-+Cl2=Br2+2Cl-.
②棉花中浸有的NaOH溶液的作用是(用离子方程式表示)Cl2+2OH-=Cl-+ClO-+H2O.
③为验证溴与碘非金属性强弱:通入少量⑧的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到溶液分层,上层几乎无色,下层呈紫红色.
④VIIA族元素,非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下,电子层数增多,原子半径逐渐增大,得电子能力逐渐减弱.
2.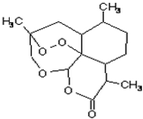 中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
 中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )| A. | 是一种烃 | B. | 属于高分子化合物 | ||
| C. | 属于芳香族化合物 | D. | 分子式是C15H22O5 |
6.下列关于元素周期表和元素周期律的说法不正确的是( )
| A. | 从氟到碘,其氢化物的稳定性逐渐减弱 | |
| B. | 氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 | |
| C. | 第三周期从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 | |
| D. | 因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 |
13.某有机物的结构简式为 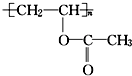 ,下列关于该有机物叙述不正确的是( )
,下列关于该有机物叙述不正确的是( )
 ,下列关于该有机物叙述不正确的是( )
,下列关于该有机物叙述不正确的是( )| A. | 1 mol 该有机物与 NaOH 溶液完全反应时,消耗 NaOH 1 mol | |
| B. | 该有机物水解所得产物能发生取代反应 | |
| C. | 该有机物可通过加聚反应生成 | |
| D. | 该有机物分子中含有双键 |
10.若从溴水中把溴萃取出来,可选用的萃取剂是( )
| A. | 水 | B. | 无水酒精 | C. | 四氯化碳 | D. | 氢氧化钠溶液 |
7.某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是( )
| A. | K+、Ca2+、HCO3-、Cl- | B. | Na+、K+、Cl-、SO42- | ||
| C. | NH4+、K+、Cl-、SO32- | D. | K+、Cl-、NO3-、SO42- |
 .
.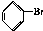 与Br2,要想得到纯净的产物,可用NaOH溶液或水试剂洗涤.
与Br2,要想得到纯净的产物,可用NaOH溶液或水试剂洗涤.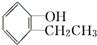 酚
酚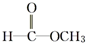 酯
酯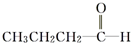 醛
醛