题目内容
6.实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸,反应如图1: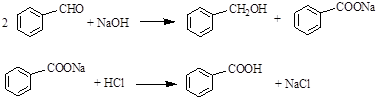
已知:
①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃).
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸.
③石蜡油沸点高于250℃
④苯甲醇沸点为205.3℃
实验步骤如下:
①向图2所示装置中加入8g氢氧化钠和30mL水,搅拌溶解,稍冷,加入10mL苯甲醛.开启搅拌器,调整转速,使搅拌平稳进行,加热回流约40min.
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温.然后用乙醚萃取三次,每次10mL.水层保留待用.合并三次萃取液,依次用5mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10mL水洗涤,然后分液,将水层弃去,所得醚层进行实验步骤③.
③将分出的醚层,倒入干燥的锥形瓶中,加无水硫酸镁,注意锥形瓶上要加塞;将锥形瓶中溶液转入图3所示的蒸馏装置,先缓缓加热,蒸出乙醚;蒸出乙醚后必须改变加热方式、冷凝方式,继续升高温度并收集205℃~206℃的馏分得产品A.
④将实验步骤②中保留待用的水层慢慢地加入到盛有30mL浓盐酸和30mL水的混合物中,同时用玻璃棒搅拌,析出白色固体.冷却,抽滤,得到粗产品,然后提纯得产品B.
根据以上步骤回答下列问题:
(1)步骤②萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需分液漏斗(仪器名称).
(2)步骤②中饱和亚硫酸氢钠溶液洗涤是为了除去未反应完的苯甲醛,而用碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸.醚层中少量的苯甲酸是从水层转移过来的,请用离子方程式说明其产生的原因
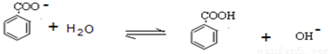 .
.(3)步骤③中无水硫酸镁的作用是吸收水分,锥形瓶上要加塞的原因是防止乙醚挥发与空气混合,发生爆炸,产品A为苯甲醇.
(4)步骤③中蒸馏除去乙醚的过程中采用的加热方式为水浴加热;蒸馏得产品A的加热方式是石蜡油油浴加热.
(5)步骤④中提纯产品B时所用到的实验方法为重结晶.

分析 (1)萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需分液漏斗;
(2)②中合并三次萃取后的萃取液中含有产品苯甲醇、未反应的苯甲醛,及少量从水层转移过来的苯甲酸,碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸,苯甲酸是苯甲酸钠水解生成的;用水洗去可溶性杂质,饱和亚硫酸氢钠溶液洗涤目的是洗去未反应的苯甲醛;
(3)无水硫酸镁是干燥剂;题目信息中,乙醚易挥发,与空气混合易发生爆炸,蒸馏时应防止挥发到空气中;题目信息中,苯甲醇沸点为205.3℃,收集205℃~206℃的馏分得产品应是苯甲醇;
(4)题目信息中,乙醚沸点34.6℃,蒸馏除乙醚的过程中采用的加热方式应用水浴加热;石蜡油沸点高于250℃,蒸馏得产品A,应控制温度高于苯甲醇的沸点,用石蜡油油浴加热;
(5)实验步骤②中保留待用水层中主要含有苯甲酸钠,慢慢地加入到盛有浓盐酸和水的混合物中,析出白色固体为苯甲酸,由于苯甲酸溶解度受温度影响较大,可以利用重结晶方法进行提纯.
解答 解:(1)萃取时用到的玻璃仪器除了烧杯、玻璃棒外,还需分液漏斗,故答案为:分液漏斗;
(2)②中合并三次萃取后的萃取液中含有产品苯甲醇、未反应的苯甲醛,及少量从水层转移过来的苯甲酸,碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸,苯甲酸是苯甲酸钠水解生成的,反应离子方程式为: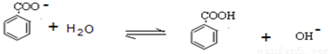 ;用水洗去可溶性杂质,故饱和亚硫酸氢钠溶液洗涤目的是洗去未反应的苯甲醛,
;用水洗去可溶性杂质,故饱和亚硫酸氢钠溶液洗涤目的是洗去未反应的苯甲醛,
故答案为:未反应完的苯甲醛;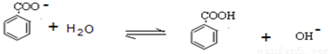 ;
;
(3)加无水硫酸镁的作用是吸收水分,起到干燥的作用;
题目信息中,乙醚易挥发,与空气混合易发生爆炸,蒸馏时锥形瓶上要加塞防止挥发到空气中;
题目信息中,苯甲醇沸点为205.3℃,收集205℃~206℃的馏分得产品应是苯甲醇,
故答案为:吸收水分;防止乙醚挥发与空气混合,发生爆炸;苯甲醇;
(4)题目信息中,乙醚沸点34.6℃,蒸馏除乙醚的过程中采用的加热方式应用水浴加热;石蜡油沸点高于250℃,蒸馏得产品A,应控制温度高于苯甲醇的沸点,用石蜡油油浴加热,
故答案为:水浴加热;石蜡油油浴加热;
(5)实验步骤②中保留待用水层中主要含有苯甲酸钠,慢慢地加入到盛有30mL浓盐酸和30mL水的混合物中,同时用玻璃棒搅拌,析出白色固体为苯甲酸,冷却,抽滤,得到粗产品,由于苯甲酸溶解度受温度影响较大,可以利用重结晶方法进行提纯,
故答案为:重结晶.
点评 本题考查有机物制备实验,侧重考查学生对原理及操作的分析评价、物质的分离提纯等,关键是充分利用题目给予的信息进行解答,较好的考查学生分析推理能力、知识迁移运用能力,题目难度中等.

 英才计划期末调研系列答案
英才计划期末调研系列答案| A. | 若正反应是吸热反应,则A为非气态 | B. | 若正反应是吸热反应,则A为气态 | ||
| C. | 若正反应是放热反应,则A为气态 | D. | 若正反应是放热反应,则A为非气态 |
| A. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| B. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用氯化铁溶液腐蚀印刷线路板上的铜:Fe3++Cu═Fe2++Cu2+ | |
| D. | 向亚硫酸钡固体中加入稀硝酸:3BaSO3+2H++2NO3-═3BaSO4↓+2NO↑+H2O |
Ⅰ、利用废液再生刻蚀液
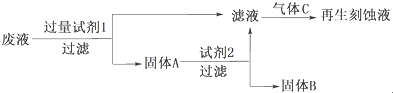
(1)试剂2是HCl,固体B是Cu,通入的气体C是Cl2.(填化学式)
(2)写出加入试剂1发生反应的离子方程式:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu.
Ⅱ、利用废液制备CuCl2•2H2O晶体
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |

(1)为确保产品的纯度,试剂1为B,试剂2为D(填字母).
A.KMnO4 B.H2O2 C.NaOH D.Cu2(OH)2CO3
(2)固体A的化学式为Fe(OH)3.为使A完全沉淀,调节pH的范围是[3.7,5.4).
(3)操作Ⅰ依次为加热浓缩、冷却结晶、过滤.操作Ⅰ整个过程中用到的硅酸盐仪器除了漏斗、烧杯、酒精灯外,还需要蒸发皿、玻璃棒.
(4)使用无水乙醇代替水进行洗涤的优点是减少CuCl2•2H2O 因溶于水而损失,且有利于后续干燥.
| A. | 凡金属元素与非金属元素之间都形成离子键 | |
| B. | 形成离子键的微粒必须是金属阳离子与阴离子 | |
| C. | 含有离子键的化合物中,也可能还含有共价键 | |
| D. | 非金属元素形成的化合物一定不存在离子键 |
| A. | 滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- | |
| B. | [H+]=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、Br- | |
| C. | [OH-]/[H+]=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| D. | 由水电离的[H+]=1.0×10-13 mol•L-1的溶液中:K+、NH4+、[Al(OH)4]-、HCO3- |

