题目内容
16.(1)我国酸雨属SO2污染型.某校兴趣小组取雨水样品进行实验.每隔一段时间测定雨水的pH,得到的结果如下表| 测定时间/h | 0 | 1 | 2 | 3 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
(2)下列一组能减少酸雨产生的有效措施是B(填字母).
①少用煤作燃料 ②加大石油、煤炭的开采速度,增加化石燃料的供应量
③燃料脱硫 ④在已酸化的土壤中加入石灰 ⑤开发新能源
A.①②⑤B.①③⑤C.②③④D.③④⑤
(3)氯系消毒剂是目前使用最广泛的一类消毒剂.家庭使用漂白粉进行消毒时,可直接将漂白粉置于空气中,请写出反应的化学方程式Ca(ClO)2+CO2+H2O═CaCO3+2HClO.
分析 (1)利用氧化还原反应来分析,亚硫酸易被氧化;
(2)煤、石油燃烧时能生成大量的二氧化硫、氮氧化物等物质,这些物质溶于水能生成显酸性的物质,当达到达到一定程度时就形成酸雨,;
(3)漂白粉的有效成分是次氯酸钙,与二氧化碳水反应生成次氯酸.
解答 解:(1)因亚硫酸易被氧化生成硫酸,酸性增强,所以pH减小,发生的反应方程式为:2H2SO3+O2=2H2SO4或2SO2+2H2O+O2=2H2SO4,
故答案为:2H2SO3+O2=2H2SO4或2SO2+2H2O+O2=2H2SO4;
(2)①少用煤作燃料、③燃料脱硫、⑤开发新能源都能够减少二氧化硫的排放,是减少酸雨产生的有效措施,而②加大石油、煤炭的开采速度,增加化石燃料的供应量,会增加二氧化硫的排放量,容易加重酸雨的形成,而④在已酸化的土壤中加入石灰,是治理土壤酸化,与酸雨的无关,
故答案为:B;
(3)漂白粉中的次氯酸钙与空气中的二氧化碳及水发生反应,生成碳酸钙和次氯酸,该反应的化学方程式为:Ca(ClO)2+CO2+H2O═CaCO3+2HClO;
故答案为:Ca(ClO)2+CO2+H2O═CaCO3+2HClO.
点评 本题考查了二氧化硫的污染及治理、漂白粉的组成及性质,题目难度中等,明确常见物质的性质为解答关键,注意掌握漂白粉的漂白原理及二氧化硫的治理方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 某无色溶液中:Al3+、Cu2+、SO42-、Cl- | |
| B. | 由水电离的c(H+)=1×10-12 mol•L-1的溶液中:Fe2+、K+、Cl-、NO3- | |
| C. | c(H+)c(OH−)=1012的溶液中:Na+、Mg2+、NO3-、Cl- | |
| D. | 含有大量HCO3-的溶液中:NH4+、Al3+、Ca2+、Cl- |
4.甲烷燃烧和氢气燃烧的热化学方程式如下:
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
2H2(g)+O2(g)=2H2O(l)△H3
常温下取体积为4:1的甲烷和氢气混合气体11.2L(标况),完全燃烧后恢复常温,放出热量为( )
CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
2H2(g)+O2(g)=2H2O(l)△H3
常温下取体积为4:1的甲烷和氢气混合气体11.2L(标况),完全燃烧后恢复常温,放出热量为( )
| A. | 0.4△H1+0.05△H3 | B. | 0.4△H1+0.05△H2 | C. | 0.4△H1+0.1△H3 | D. | 0.4△H1+0.2△H3 |
11.下列各组元素的性质递变情况错误的是( )
| A. | Li、C、O原子最外层电子数依次增加 | B. | P、S、Cl元素最高正化合价依次升高 | ||
| C. | N、O、F原子半径依次增大 | D. | Li、Na、K的金属性依次增强 |
8.已知:t℃时,2H(g)+Y(g)?2I(g)△H=-196.6kJ•mol-1,t℃时,在一压强恒定的密闭容器中,加入4mol H和2mol Y反应,达到平衡后,Y剩余0.2mol.若在上面的平衡体系中,再加入1mol气态的I物质,t℃时达到新的平衡,此时H物质的物质的量n(H)为( )
| A. | 0.8 mol | B. | 0.6 mol | C. | 0.5 mol | D. | 0.2 mol |
6.现有下列短周期元素性质的数据:
试回答下列问题:
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或 最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)元素③在周期表中的位置是第二周期第ⅠA族;元素①②④⑦的气态氢化物中最稳定的是H2O(填化学式);
(2)上述元素形成的单核离子中半径最大的是P3-,半径最小的是Li+;
(3)元素①与元素⑥按照原子个数比为1:1形成的化合物与水反应的化学反应方程式2Na2O2+2H2O═4NaOH+O2↑;
(4)元素⑤形成的单质加入到元素②的氢化物的水溶液中,反应生成两种强酸的离子方程式4Cl2+H2S+4H2O═10H++8Cl-+SO42-.
 已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应.甲是常见的黑色固体单质,乙是常见的气体单质,是空气的主要成分之一,B是无色气体,是主要的大气污染物之一,C常温下为无色液体,E是一种淡黄色的固体.请回答下列问题.
已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应.甲是常见的黑色固体单质,乙是常见的气体单质,是空气的主要成分之一,B是无色气体,是主要的大气污染物之一,C常温下为无色液体,E是一种淡黄色的固体.请回答下列问题.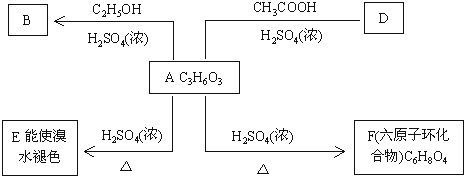

 .
.