��Ŀ����
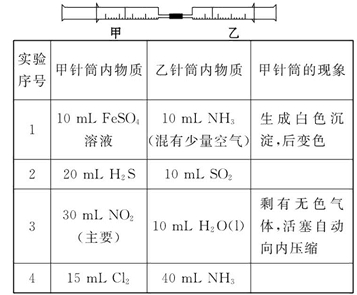
����ͼ��ʾװ�ý���ʵ��(�г�װ������ȥ)����ش���������:
(1)��A��ΪŨ����,B��Ϊͭ����,C��Ϊ����������Һ����Ũ�������B��,��B�з�����Ӧ�Ļ�ѧ����ʽΪ��
(2)��A��ΪŨ��ˮ,B��Ϊ��ʯ��,C��Ϊ������Һ��
�ٽ�Ũ��ˮ��ε���B��,�ɲ�����������,ԭ�������(�����)��
a.��ʯ�Һ�Ũ��ˮ��Ӧ��������,����������ˮ
b.��ʯ�Һ�ˮ��Ӧ,����ˮ,ʹ�������ܽ�������
c.��Ӧ�ų�������,ʹ������ˮ�е��ܽ�����Խ���
��C��ͨ���������ʱ����Ӧ�����ӷ���ʽΪ��
(3)��A��Ϊˮ,B��Ϊ��������,C��Ϊ���Ե��۵⻯����Һ,��ˮ����B�к�,B�е�ʵ������Ϊ;��C����Һ��Ϊ��ɫ,��C�з�����Ӧ�����ӷ���ʽΪ��
��1��3Cu+8HNO3(Ũ)=3Cu(NO3)2+2NO2��+4H2O.(2) ��bc. ��Al3++3NH3��H2O=Al(OH)3��+3NH4+��3Al3++3NH3+3H2O=Al(OH)3��+3NH4+��3��ð���ݣ�������ɫ���壬ˮ��ҺΪ��ɫ��4H++4I-+O2=2I2+2H2O.
�������������(1)������ǿ�������ԣ�������������õĽ�����Ӧ��Ҳ�����벻���õĽ�����Ӧ��Ũ������ͭ��Ӧ�ķ���ʽΪ3Cu+8HNO3(Ũ)=3Cu(NO3)2+2NO2��+4H2O.(2) �ٽ�Ũ��ˮ��ε�����ʯ����,������ʯ�Һ�ˮ��Ӧ,����ˮ,ʹ�������ܽ��������Լ���Ӧ�ų�������,ʹ������ˮ�е��ܽ�����Խ��ͣ��ʿɲ�������������ѡ��Ϊbc. �ڵ���������Һ��ͨ���������ʱ������Ӧ�����ӷ���ʽΪ��Al3++3NH3��H2O=Al(OH)3��+3NH4+��Ϊ3Al3++3NH3+3H2O=Al(OH)3��+3NH4+��3�������A��Ϊˮ,B��Ϊ��������,��ˮ����B�к�,B�е�ʵ������Ϊð���ݣ�������ɫ���壬ˮ��ҺΪ��ɫ��C��Ϊ���Ե��۵⻯����Һ,��C����Һ��Ϊ��ɫ,��C�з�����Ӧ�����ӷ���ʽΪ��4H++4I-+O2=2I2+2H2O.
���㣺�������ᡢ������������������������ʻ�ѧ���ʵ���ص�֪ʶ��

 ��У����ϵ�д�
��У����ϵ�д�һ�ֺ�����ﮡ��ܵ����͵��Ӳ��ϣ������в����ķ��������ɹۣ������е����Խ�����������ʽ���ڣ�����Co2O3��CoO����ʽ���ڣ������������ĵ����˫�棻﮻��������С�
�ӷ����л��������ܣ�CoO���Ĺ����������£�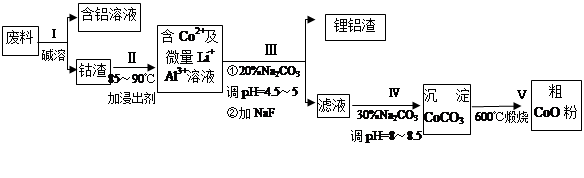
��1������I�в���NaOH��Һ�ܳ������е�Al����Ӧ�����ӷ���ʽΪ ��
��2������II�м���ϡH2SO4�ữ���ټ���Na2S2O3��Һ�����ܡ�������ܵĻ�ѧ��Ӧ����ʽΪ��������ֻ��һ������� ����ʵ����ģ�ҵ����ʱ��Ҳ������������ܣ���ʵ�ʹ�ҵ�����в������ᣬ��ӷ�Ӧԭ������������������ܵ���Ҫԭ��_______________��
��3�����̢�õ����������Ҫ�ɷ���LiF��Al(OH)3��̼������Һ�ڲ���Al(OH)3ʱ����Ҫ���ã���д���÷�Ӧ�����ӷ���ʽ____________________��
��4��̼������Һ�ڹ���III��IV����������������ͬ����д���ڹ���IV�����������__________��
��5����Na2CO3��Һ�д��ڶ������ӣ����и�����Ũ�ȹ�ϵ��ȷ����______������ţ���
| A��c(Na+) = 2c(CO32-) |
| B��c(Na+) > c(CO32-) > c(HCO3-) |
| C��c(OH-) > c(HCO3-) > c(H+) |
| D��c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3) |
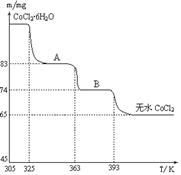
ͬλ��2H��15N��18O��34S�ȳ�������½����̬�����о�������˵������ȷ����
| A��16O��18O��ͬһ�ֺ��� | B�� 1H218O��Ħ������Ϊ20 |
| C��34S��15N���ڵ����������9 | D��2H�����������Ϊ0 |
����˵����ȷ���ǣ� ��
| A��������Ʒ¶�����һ��ʱ�䣬������ǿ����������ˮ�����ɷֱ�������ԭ�� |
| B��CH4��NH3��PH3�����ȶ�������ǿ |
| C����Ϊ���ԣ�HC1>HF�����Էǽ����ԣ�Cl>F |
| D����ԭ���ڷ�Ӧ��ʧȥ�ĵ��ӱ���ԭ���٣����ƵĽ����Ա����� |
ijԪ��ԭ�ӵ��������1�����ӣ����Ԫ�ز�������
| A��IA��Ԫ�� | B������Ԫ�� | C���ǽ���Ԫ�� | D������Ԫ�� |
���ݱ�����Ϣ���ж�����������ȷ����( )
���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ�
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶��nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| ��Ҫ���ϼ� | ��2 | ��3 | ��2 | ��6����2 | ��2 |
C��M��T�γɵĻ������������ D��L2+��R2���ĺ�����������