题目内容
同位素2H、15N、18O、34S等常被用做陆地生态分析研究。下列说法中正确的是
| A.16O和18O是同一种核素 | B. 1H218O的摩尔质量为20 |
| C.34S和15N核内的中子数相差9 | D.2H+核外电子数为0 |
D
解析试题分析:A、16O和18O的质子数都为8,中子数分别为8、10,不是同一种核素,故A错误;B、1H218O的摩尔质量为20g/mol,故B错误;C、34S和15N核内的中子数分别为34-16=18,15-7=8,中子数相差10,故C错误;D、2H+核外电子数为1-1=0,故D正确;故选:D。
考点:考查原子符号的含义,中子数=质量数-质子数以及离子中核外电子数目的计算

练习册系列答案
相关题目
有关元素X、Y、Z、D、E的信息如下:
| | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074 nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102 nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物可溶于水,且能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为___________。
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)_______。
①保存EY2溶液时,需向溶液中加入少量E单质
②EY2只能通过置换反应生成,EY3只能通过化合反应生成
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
(3)将Z单质在X的单质中燃烧的产物和等物质的量的Y单质同时通入足量的水中,充分反应后的溶液中滴入品红溶液,现象是__________________,有关反应的离子方程式为________________________________________________________________________。
已知下列元素的原子半径:
| 元素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
A.0.80×10-10 m B.1.10×10-10 m C.1.20×10-10 m D.0.70×10-10 m
 下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是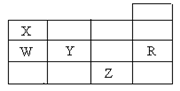
| A.常压下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物比X的氢化物稳定 |
| D.Y元素最高价氧化物对应水化物比W元素的最高价氧化物对应水化物的酸性强 |
对元素周期表和元素周期律的发现有突出贡献的科学家是
| A.拉瓦锡 | B.门捷列夫 | C.阿伏加德罗 | D.道尔顿 |
下列叙述中正确的是 ( )
| A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| B.除短周期外,其它周期均有18种元素 |
| C.在同一周期中,ⅠA族比ⅡA族的单质与水反应更剧烈 |
| D.在ⅠA族中,单质的熔、沸点随着原子半径的增大而逐渐升高 |