题目内容
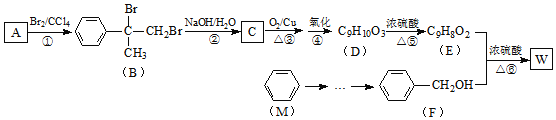
【题目】铋及其化合物在工业生产中用途广泛,某研究小组用浮选过的辉铋矿![]() 主要成分是
主要成分是![]() ,还含少量
,还含少量![]() 等杂质
等杂质![]() 制备
制备![]() ,其流程如下:
,其流程如下:

已知:![]() 水解能力:
水解能力:![]()
![]() 。
。
回答下列问题:
(1)“浸取”时,为了提高浸取速率,可采取的措施有___________![]() 任写一条
任写一条![]() ;过滤1的滤渣的主要成分有______________
;过滤1的滤渣的主要成分有______________![]() 填化学式
填化学式![]() 。
。
(2)浸取时加入过量浓盐酸的目的是____________________________________。
(3)写出焙烧时生成铋酸钠的化学方程式_________________________________。
(4)![]() 时,向浓度均为
时,向浓度均为![]() 的
的![]() 、
、![]() 的混合溶液中滴加
的混合溶液中滴加![]() 溶液
溶液![]() 设溶液体积增加1倍
设溶液体积增加1倍![]() ,当
,当![]() 时恰好完全沉淀,判断此时
时恰好完全沉淀,判断此时![]() 是否已经开始沉淀________
是否已经开始沉淀________![]() 填“是”或“否”
填“是”或“否”![]() 已知:
已知:![]() 、
、![]()
(5)用双硫腙![]() ,二元弱酸
,二元弱酸![]() 络合萃取法可从工业废水中提取金属离子:
络合萃取法可从工业废水中提取金属离子:![]() 先将金属离子络合成电中性的物质
先将金属离子络合成电中性的物质![]() 如
如![]() 等
等![]() ,再用
,再用![]() 萃取此络合物。下图是用上述方法处理含有
萃取此络合物。下图是用上述方法处理含有![]() 、
、![]() 、
、![]() 的废水时的酸度曲线
的废水时的酸度曲线![]() 表示金属离子以络合物形式被萃取分离的百分率
表示金属离子以络合物形式被萃取分离的百分率![]() 。
。
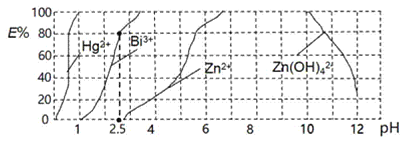
![]() 当调节
当调节![]() 时,铋
时,铋![]() 的存在形式为____________。
的存在形式为____________。
![]() 向萃取后的
向萃取后的![]() 中加入过量NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为____。
中加入过量NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为____。
【答案】粉碎矿石、适当提高浸取时温度、适当提高溶液浓度、搅拌等![]() 任写一条
任写一条![]() S、
S、![]() 防止
防止![]() 及
及![]() 水解生成不溶性沉淀,提高原料的浸出率 2Bi+2O2+Na2O2
水解生成不溶性沉淀,提高原料的浸出率 2Bi+2O2+Na2O2![]() 2NaBiO3 否
2NaBiO3 否 ![]() 、
、![]()
![]()
【解析】
辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)制备NaBiO3,辉铋矿加入盐酸酸溶浸取,二氧化硅不溶解,加入氯化铁溶液氧化硫离子生成单质硫,过滤得到滤渣为二氧化硅和硫单质,滤液中加入Fe还原铁离子过滤得到粗铋,精炼后的铋通入氧气加入过氧化钠发生反应生成NaBiO3,以此解答该题。
(1)浸取”时,粉碎矿石、适当提高浸取时温度、适当提高FeCl3溶液浓度、浸取时不断搅拌等都可以加快浸取速率;滤渣1中含有的SiO2和铁离子氧化硫离子生成的单质硫,化学式为:S、SiO2;
(2)![]() 溶于浓盐酸,铁离子、铋离子易发生水解,加入浓盐酸可溶解
溶于浓盐酸,铁离子、铋离子易发生水解,加入浓盐酸可溶解![]() ,同时防止
,同时防止![]() 及
及![]() 水解生成不溶性沉淀,从而提高原料的浸出率;
水解生成不溶性沉淀,从而提高原料的浸出率;
(3)金属Bi与氧气、过氧化钠焙烧生成铋酸钠,该反应的化学方程式为:![]() ;
;
(4)体积增大一倍,浓度减小到原来的二分之一,![]() ,当c(Pb2+)=10-5mol/L时恰好完全沉淀,c(S2-)=
,当c(Pb2+)=10-5mol/L时恰好完全沉淀,c(S2-)=![]() ,Qc(Bi2S3)= c2(Bi3+) c3(S2-)=(0.02)2×(
,Qc(Bi2S3)= c2(Bi3+) c3(S2-)=(0.02)2×(![]() )3<1.6×10-20,可知
)3<1.6×10-20,可知![]() 离子不沉淀;
离子不沉淀;
(5)![]() 当调节
当调节![]() 时铋的萃取率是80%,铋
时铋的萃取率是80%,铋![]() 的存在形式有:
的存在形式有:![]() 、
、![]() ;
;
![]() 向萃取后的
向萃取后的![]() 中加入NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,该沉淀为
中加入NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,该沉淀为![]() ,反应的离子方程式为:
,反应的离子方程式为:![]() 。
。

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案