题目内容
2.某学生往一支试管里按一定次序分别加入下列几种溶液:A.KI溶液 B.淀粉溶液 C.NaOH溶液 D.氯水
发现溶液颜色按下列次序变化
①无色$\stackrel{加入②}{→}$棕黄色$\stackrel{加入③}{→}$蓝色$\stackrel{加入④}{→}$无色
依据溶液颜色的变化,回答下列问题:
(1)加入以上药品的顺序是A、D、B、C;
(2)写出加入试剂②的离子反应方程式,若为氧化还原反应,请标明电子转移的方向和数目:
 ;
;(3)写出加入试剂④的化学方程式:I2+2NaOH═NaI+NaIO+H2O.
分析 发现溶液颜色按下面次序变化:①无色→②棕黄色→③蓝色→④无色,则先加KI溶液,再加氯水发生氧化还原反应生成碘,然后加淀粉,最后加NaOH溶液发生反应生成NaI、NaIO,以此来解答.
解答 解:发现溶液颜色按下面次序变化:①无色→②棕黄色→③蓝色→④无色,则先加KI溶液,再加氯水发生氧化还原反应生成碘,然后加淀粉,最后加NaOH溶液发生反应生成NaI、NaIO,
(1)由上述分析可知,试剂的加入顺序为A、D、B、C,故答案为:A、D、B、C;
(2)①→②的离子反应方程式及电子转移的方向和总数为 ,故答案为:
,故答案为: ;
;
(3)③→④的化学反应方程式为I2+2NaOH═NaI+NaIO+H2O,故答案为:I2+2NaOH═NaI+NaIO+H2O.
点评 本题考查物质的性质及氧化还原反应,为高频考点,把握颜色变化与发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
12.下列叙述中,不正确的是( )
| A. | 元素金属性:Al<Mg<Na | B. | 元素非金属性:F>Cl>Br | ||
| C. | 酸性:HClO4<H2SO4<H3PO4 | D. | 气态氢化物稳定性:HF>HCl>H2S |
17.下面三种方法都可以制得氯气.
①MnO2+4HCl(浓)═MnCl2+Cl2+2H2O
②2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2+8H2O
③4HCl(浓)+O2$\frac{\underline{催化剂}}{△}$2H2O+Cl2
这三种氧化剂的氧化性由强到弱的顺序是( )
①MnO2+4HCl(浓)═MnCl2+Cl2+2H2O
②2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2+8H2O
③4HCl(浓)+O2$\frac{\underline{催化剂}}{△}$2H2O+Cl2
这三种氧化剂的氧化性由强到弱的顺序是( )
| A. | O2>MnO2>KMnO4 | B. | KMnO4>MnO2>O2 | C. | MnO2>KMnO4>O2 | D. | O2>MnO2>KMnO4 |
7.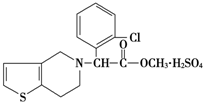 波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
 波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )| A. | 该物质的化学式为C16H15ClNO2•H2SO4 | |
| B. | 该物质难溶于水 | |
| C. | 波立维能形成硫酸氢盐是与其结构中的氮原子有关 | |
| D. | 它可以与NaOH溶液反应,1 mol该物质最多可消耗2mol NaOH |
14.下列关于微粒之间作用力的说法正确的是( )
| A. | 在分子中,化学键可能只有π键,而没有σ 键 | |
| B. | 不同元素组成的多原子分子里的化学键一定都是极性键 | |
| C. | 实验测得NO2和CH3COOH 的摩尔质量均比理论值大,可能原因是在实验条件下这两种分子均能发生“双聚”,这种分子“双聚”的作用力是相同类型的作用力 | |
| D. | 原子晶体的熔点一定比分子晶体高,原因之一是共价键是一种比分子间作用力更为强烈的相互作用 |
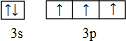 ;
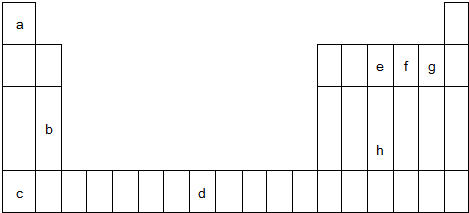
;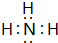 ,其分子的空间构型是三角锥形,分子中e原子的杂化类型是sp3.
,其分子的空间构型是三角锥形,分子中e原子的杂化类型是sp3. 2-甲基丁烷;(2)
2-甲基丁烷;(2) 2,2-二甲基丙烷.
2,2-二甲基丙烷.
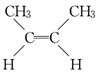 (顺式2-丁烯)、
(顺式2-丁烯)、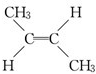 (反式2-丁烯);
(反式2-丁烯);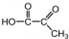 ,B.可与足量H2加成得到2-甲基戊烷,请写出B的结构简式CH3CH=CHC(CH3)=CHCH3;写出B发生加聚反应的方程式
,B.可与足量H2加成得到2-甲基戊烷,请写出B的结构简式CH3CH=CHC(CH3)=CHCH3;写出B发生加聚反应的方程式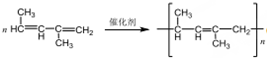 .
.