题目内容
14.下列关于微粒之间作用力的说法正确的是( )| A. | 在分子中,化学键可能只有π键,而没有σ 键 | |
| B. | 不同元素组成的多原子分子里的化学键一定都是极性键 | |
| C. | 实验测得NO2和CH3COOH 的摩尔质量均比理论值大,可能原因是在实验条件下这两种分子均能发生“双聚”,这种分子“双聚”的作用力是相同类型的作用力 | |
| D. | 原子晶体的熔点一定比分子晶体高,原因之一是共价键是一种比分子间作用力更为强烈的相互作用 |
分析 A.共价单键为σ键,而双键和三键中含σ键、π键;
B.化合物中如存在相同原子之间的形成的化学键,则为非极性键;
C.实验测得NO2和CH3COOH 的摩尔质量均比理论值大,NO2因为发生可逆反应生成四氧化二氮,CH3COOH因为分子间的氢键“双聚”;
D.原子晶体熔化破坏的是共价键,分子晶体熔化破坏的是分子间作用力.
解答 解:A.共价键中一定含σ键,则在分子中,化学键可能只有σ键,而没有π键,故A错误;
B.H2O2,Na2O2为不同元素组成的多原子分子,存在非极性键,故A错误;
C.实验测得NO2和CH3COOH 的摩尔质量均比理论值大,NO2因为发生可逆反应生成四氧化二氮,CH3COOH因为分子间的氢键“双聚”,则作用力是不同类型的作用力,故C错误;
D.原子晶体熔化破坏的是共价键,分子晶体熔化破坏的是分子间作用力,共价键比分子间作用力强度大,所以原子晶体的熔点一定比分子晶体高,故D正确.
故选D.
点评 本题考查共价键及类型以及微粒之间的作用力的分析,为高频考点,把握共价键的形成及判断共价键的规律为解答的关键,注意共价键中一定含σ键,题目难度中等,侧重分子结构与性质的考查.

练习册系列答案
相关题目
4.下列试剂,必须用棕色瓶盛装的是( )
①浓氨水 ②氯水 ③硝酸银 ④浓硝酸 ⑤浓盐酸 ⑥溴化银.
①浓氨水 ②氯水 ③硝酸银 ④浓硝酸 ⑤浓盐酸 ⑥溴化银.
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③⑤⑥ | D. | ①③④⑥ |
5.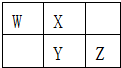 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可使湿润的红色石蕊试纸变蓝,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可使湿润的红色石蕊试纸变蓝,由此可知( )
 W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可使湿润的红色石蕊试纸变蓝,由此可知( )
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可使湿润的红色石蕊试纸变蓝,由此可知( )| A. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| B. | Z元素氧化物对应水化物的酸性一定强于Y | |
| C. | W元素形成的单核阴离子半径小于X元素形成的单核阴离子半径 | |
| D. | Z元素单质在化学反应中只表现氧化性 |
3.根据元素的单质和化合物的性质,判断元素非金属性强弱的依据一般是( )
| A. | 元素最高价氧化物对应的水化物的碱性的强弱 | |
| B. | 元素氧化物对应的水化物的酸性的强弱 | |
| C. | 元素的单质与氢气反应生成气态氢化物的难易 | |
| D. | 元素的单质与酸反应置换出氢的难易 |
10.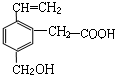 某有机物的结构简式如图,该物质应有的化学性质是( )
某有机物的结构简式如图,该物质应有的化学性质是( )
①可燃烧;
②可跟溴加成;
③可使酸性KMnO4溶液褪色;
④可跟NaHCO3溶液反应
⑤可跟Cu(OH)2反应;
⑥可跟金属钠反应
⑦可生成高分子化合物.
 某有机物的结构简式如图,该物质应有的化学性质是( )
某有机物的结构简式如图,该物质应有的化学性质是( )①可燃烧;
②可跟溴加成;
③可使酸性KMnO4溶液褪色;
④可跟NaHCO3溶液反应
⑤可跟Cu(OH)2反应;
⑥可跟金属钠反应
⑦可生成高分子化合物.
| A. | ①②③⑥ | B. | ②③④⑥ | C. | ①②③④⑤⑥⑦ | D. | ②③④⑥ |
8.下列是四种烷烃分子的结构模型图,其中沸点最高的是( )
| A. |  | B. | 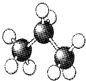 | C. | 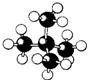 | D. | 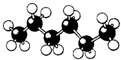 |
 ;
;