��Ŀ����
9���²��ϵ��з��Ƿ�չ�¼���������������������ʻ��������������һ�����Ͷ�ܲ��ϣ�������ص��Ʊ���
�ٷ���һ��������������
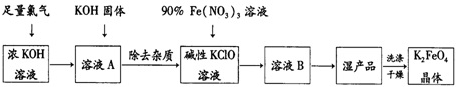
��1����ҺA�м���KOH�����Ŀ���ǣ�AD��������ţ�
A��Ϊ��һ����Ӧ�ṩ���Ի���
B��ʹKClO3ת����KClO
C���ӹ���KOH�ܽ�ʱ�ų�������������߷�Ӧ����
D������ҺA��Cl2����������Ӧ���ɸ���KClO
��2����ҺA�����ȥ������������Cl-�������ӷ���ʽ��ʾ�����ɵ�ԭ��Cl2+2OH-=Cl-+ClO-+H2O��
��3����ҺB�пɷ����ʪ��ƷK2FeO4�⣬���и�����KNO3��KCl��д��������ҺB�����ӷ���ʽ��3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O��ÿ�Ƶ�118.8gK2FeO4����������������0.9mol��
�ڷ���������ⷨ
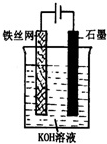
�ӻ��������Ƕȿ����Ʊ�������ؽϺ÷���Ϊ��ⷨ����װ����ͼ�������۷���K2FeO4Ӧ���������ɣ�����������������õ缫�ĵ缫����ʽΪFe+8OH--6e-=FeO42-+4H2O��
������ص�Ӧ�ã�
���������һ�����Ͷ��ε�أ����ҺΪ������Һ���䷴ӦʽΪ��
3Zn��OH��2+2Fe��OH��3+4KOH- $\frac{\underline{\;���\;}}{�ŵ�}$3Zn+2K2FeO4+8H2O
�ŵ�ʱ���缫��ӦʽΪ��������3Zn-6e-+6OH-=3Zn��OH��2 ������2FeO42-+6e-+8H2O=2Fe��OH��3+10 0H-��
���� �ٷ���һ���ɹ������̿�֪��������Ũ����������Һ������Ӧ��2KOH+Cl2�TKCl+KClO+H2O���ټ����������ع��壬Ϊ��һ����Ӧ�ṩ���Ի���������Ӧ����ҺA���ܽ��������������ҺA�к�������Cl-���ӣ���Ҫ��ȥ���ڼ���KClO��Һ�м�����������Һ��Ӧ�õ�K2FeO4����ϣ�3���л��и�����KNO3��KCl��������Ӧ��3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O��
�ڷ�������FeΪ������ʧȥ���ӣ����������µõ�K2FeO4���ɵ���غ㣬Ӧ�����������Ӳ��뷴Ӧ����Ԫ���غ��֪��Ӧ��ˮ���ɣ�
�ŵ�ʱ����������������Ӧ��Znʧȥ��������Zn��OH��2��Ӧ�����������Ӳ��뷴Ӧ������������ԭ��Ӧ��FeO42-��õ�������Fe��OH��3��Ӧ��ˮ���뷴Ӧ��ͬʱ�������������ӣ�
��� �⣺�ٷ���һ���ɹ������̿�֪��������Ũ����������Һ������Ӧ��2KOH+Cl2�TKCl+KClO+H2O���ټ����������ع��壬Ϊ��һ����Ӧ�ṩ���Ի���������Ӧ����ҺA���ܽ��������������ҺA�к�������Cl-���ӣ���Ҫ��ȥ���ڼ���KClO��Һ�м�����������Һ��Ӧ�õ�K2FeO4����ϣ�3���л��и�����KNO3��KCl��������Ӧ��3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O��
��1��������������֪����ҺA�м���KOH�����Ŀ���ǣ�Ϊ��һ����Ӧ�ṩ���Ի���������ҺA��Cl2����������Ӧ���ɸ���KClO��
�ʴ�Ϊ��AD��
��2��������ҺA�����ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O����ҺA�����ȥ������������Cl-��
�ʴ�Ϊ��Cl-��Cl2+2OH-=Cl-+ClO-+H2O��
��3����ҺB�пɷ����ʪ��ƷK2FeO4�⣬���и�����KNO3��KCl��������ҺB�����ӷ���ʽ��3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O��118.8gK2FeO4�����ʵ���Ϊ$\frac{118.8g}{198g/mol}$=0.6mol������������KClOΪ0.6mol��$\frac{3}{2}$=0.9mol��
�ʴ�Ϊ��3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O��0.9mol��
�ڷ�������FeΪ������ʧȥ���ӣ����������µõ�K2FeO4���ɵ���غ㣬Ӧ�����������Ӳ��뷴Ӧ����Ԫ���غ��֪��Ӧ��ˮ���ɣ��缫��ӦʽΪ��Fe+8OH--6e-=FeO42-+4H2O��
�ʴ�Ϊ������Fe+8OH--6e-=FeO42-+4H2O��
�ŵ�ʱ����������������Ӧ��Znʧȥ��������Zn��OH��2��Ӧ�����������Ӳ��뷴Ӧ�������缫��ӦʽΪ��3Zn-6e-+6OH-=3Zn��OH��2 ��
����������ԭ��Ӧ��FeO42-��õ�������Fe��OH��3��Ӧ��ˮ���뷴Ӧ��ͬʱ�������������ӣ������缫��ӦʽΪ��2FeO42-+6e-+8H2O=2Fe��OH��3+10 0H-��
�ʴ�Ϊ��3Zn-6e-+6OH-=3Zn��OH��2 ��2FeO42-+6e-+8H2O=2Fe��OH��3+10 0H-��
���� ���⿼�������Ʊ�ʵ�鷽����ԭ��ؼ����ԭ��Ӧ�ã��ؼ��ǶԹ������̵����⣬���ؿ���ѧ������������֪ʶǨ��������������Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | 1mol�������ƻ��������������ˮ��Ӧ������0.5mol���� | |
| B�� | ���������Ļ�ѧʽ��Ba2O2 | |
| C�� | �������������ӻ����� | |
| D�� | �������ƺ�����������ǿ������ |
ʪ���Ʊ�����Ҫ��Ӧ����Ϊ��2Fe��OH��3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
�ɷ��Ʊ�����Ҫ��Ӧ����Ϊ��2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4
�����йظ÷�Ӧ��˵��������ǣ�������
| A�� | ����Ӧ��Na2FeO4��Ϊ�������� | |
| B�� | Na2FeO4��ǿ�����ԣ�������ɱ�����仹ԭ����������ˮ������ | |
| C�� | �ɷ���ÿ����1mol Na2FeO4ת��3mol���� | |
| D�� | ���������£�NaClO�����Դ���Na2FeO4 |
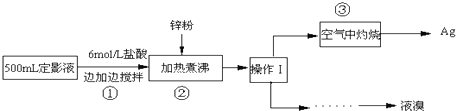
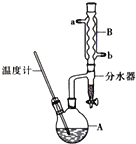 �����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵ���Ҫʵ��װ����ͼ����Ӧ��Ͳ���������������
�����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵ���Ҫʵ��װ����ͼ����Ӧ��Ͳ��������������������£�
| ��Է� ������ | �е�/ �� | �ܶ� ��g•cm-3�� | ˮ���ܽ��� | |
| ������ | 74 | 117.2 | 0.8109 | �� |
| ������ | 130 | 142.0 | 0.7704 | �������� |
�ٽ�6mLŨ�����37g����������һ��˳�����ӵ�A�У����Ӽ�����ʯ��
�ڼ���A�з�ӦҺ��Ѹ��������135�棬ά�ַ�Ӧһ��ʱ�䣬�����ᴿ��
�۴�A��Һ����ȴ���仺������ʢ��70mLˮ�ķ�Һ©���У���ҡ���ã���Һ�ôֲ��
�ֲܴ���������40mLˮ��20mL NaOH��Һ��40mLˮϴ�ӣ���Һ�����Լ3g��ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�
�ݽ������������Ĵֲ�����������ռ���֣��ô���������11g��
��ش�
��1���������Ũ�����������������˳��Ϊ��ŨH2SO4�μӵ��������У�
д����������Ʊ������ѵĻ�ѧ����ʽ2CH3CH2CH2CH2OH
 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O��
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O�� ��2������Aǰ�����ȴ�b���a����b��������B��ͨ��ˮ��
��3������۵�Ŀ���dz���ϴȥŨH2SO4����ҡ���ã��ֲ���Ӧ�ӷ�Һ©�����ϣ���ϡ����¡����ڷ������
��4������������һ��ˮϴ��Ŀ��Ϊϴȥ�л����в�����NaOH���кͷ�Ӧ���ɵ���Na2SO4��
��5��������У���������ʱӦ�ռ�d����ѡ����ĸ�����ҵ���֣�
a��100��b�� 117��c�� 135��d��142��
��6����Ӧ�����л�۲쵽��ˮ�����ռ���Һ�����ʣ��ҷ�Ϊ�������㣬���ŷ�Ӧ�Ľ��У���ˮ����Һ��������������ʱ���ϲ�Һ�������֧���Զ�����A����ˮ�����ϲ�Һ�����Ҫ�ɷ�Ϊ���������²�Һ�����Ҫ�ɷ�Ϊˮ�������������ƣ�
��7����ʵ���У������ѵIJ���Ϊ33.85%��
| A�� | CH4O��C2H4O2 | B�� | C8H10��C4H10 | C�� | C2H4��C2H4O | D�� | C8H8��C4H8O3 |
| A�� | Na+��K+��SO42-��HCO3- | B�� | Cu2+��K+��SO42-��NO3- | ||
| C�� | Fe3+��K+��SO42-��Cl- | D�� | Na+��K+��Cl-��NO3- |
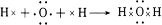 ��
�� ���������ӻ��������ӻ�����������ۻ������
���������ӻ��������ӻ�����������ۻ������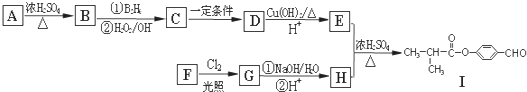
 ��
�� ��E��H��Ӧ����I�ķ���ʽΪ
��E��H��Ӧ����I�ķ���ʽΪ ��
��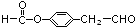 ��
��