题目内容
【题目】随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。
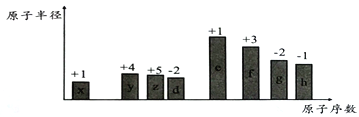
请回答下列问题:
(1)f在周期表中的位置为______________;x形成的阴离子的结构示意图为_____________________。
(2)比较d、e常见离子的半径大小:__________________(填化学式,下同);比较g、h的最高价氧化物对应水化物的酸性强弱:_______________________。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,其化学式为__________________________。
②能形成共价化合物,写出其中一种的结构简式____________________________。
【答案】 第3周期ⅢA族 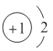 O2- > Na+ HC1O4 > H2SO4 NH4HC2O4 CO(NH2)2 (或各种氨基酸、HCNO等物质的结构简式)
O2- > Na+ HC1O4 > H2SO4 NH4HC2O4 CO(NH2)2 (或各种氨基酸、HCNO等物质的结构简式)
【解析】从图中的化合价、原子半径的大小及原子序数可知:x是H元素,y是C元素,z是N元素,d是O元素,e是Na元素,f是Al元素,g是S元素,h是Cl元素。
(1)f是Al元素,其原子序数为13,在元素周期表中位于第三周期ⅢA族,x是H元素,H-阴离子的结构示意图为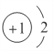 :故答案为:第三周期ⅢA族;
:故答案为:第三周期ⅢA族;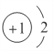 ;
;
(2)电子层结构相同的离子,核电荷数越大离子半径越小,故离子半径:O2->Na+;非金属性越强,最高价氧化物水化物的酸性越强,故酸性:HClO4>H2SO4,故答案为:O2->Na+;HClO4>H2SO4;
(3)①x、y、z、d四种元素能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶2∶1 ∶4,则该化合物的化学式为NH4HC2O4,故答案为:NH4HC2O4;
②x、y、z、d四种元素能形成共价化合物,可以是各种氨基酸或尿素等,其中尿素的结构简式为CO(NH2)2,故答案为:CO(NH2)2。

 期末集结号系列答案
期末集结号系列答案【题目】根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )
选项 | A | B | C | D |
图像 |
|
|
|
|
反应 | aX(g)+bY(g)cZ(g) | L(s)+aG(g)bR(g) | aA+bBcC | A+2B2C+3D |
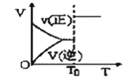
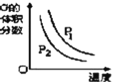
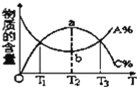
操作或条件 | 密闭容器中反应达到平衡,T0时改变某一条件有如图变化所示,则改变的条件一定是加入催化剂 | 反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应,且a>b | 物质的百分含量和温度关系如图所示,则该反应的正反应为吸热反应 | 反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C是气体,D为固体或液体 |
A.AB.BC.CD.D