题目内容
13.W、X、Y、Z为原子序数依次增大的四种短周期主族元素,在周期表中,W的原子半径是最小的,Y的最高价氧化物既能与强酸反应,又能与强碱溶液反应,X与Z位于同一主族.Z-与Ar具有相同的电子层结构,请回答下列问题:(1)写出元素符号:X为F,Y为Al.
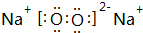
(2)用电子式表示WZ的形成过程:
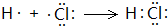 .
.(3)Y的氧化物与NaOH溶液反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O.
分析 W、X、Y、Z为原子序数依次增大的四种短周期主族元素,在周期表中,W的原子半径是最小的,则W为H元素;Y的最高价氧化物既能与强酸反应,又能与强碱溶液反应,则Y为Al;Z-与Ar具有相同的电子层结构,则Z为Cl元素;X与Z位于同一主族,则X为F元素.
解答 解:W、X、Y、Z为原子序数依次增大的四种短周期主族元素,在周期表中,W的原子半径是最小的,则W为H元素;Y的最高价氧化物既能与强酸反应,又能与强碱溶液反应,则Y为Al;Z-与Ar具有相同的电子层结构,则Z为Cl元素;X与Z位于同一主族,则X为F元素.
(1)由上述分析可知,X为F元素,Y为Al,故答案为:F;Al;
(2)用电子式表示HCl的形成过程: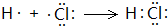 ,故答案为:
,故答案为: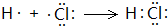 ;
;
(3)Y的氧化物为Al2O3,与NaOH溶液反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O.
点评 本题考查位置结构与性质的关系及应用,题目难度不大,推断元素为解答的关键,注意理解掌握用电子式表示物质或化学键的形成.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
4.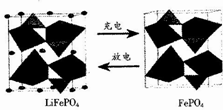 LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
 LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )
LiFePO4是锂离子电池一种电极材料,其结构稳定、资源丰富、安全性能好、无毒.该电极材料在充放电时的变化如图所示,下列有关说法正确的是( )| A. | 放电时该电极为负极 | |
| B. | 充电是Li+向阳极移动 | |
| C. | 充电时该电极发生氧化反应,反应式为LiFePO4-e-=FePO4+Li+ | |
| D. | 该电池可以用磷酸溶液作电解质 |
18.为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法错误的是( )
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
| A | KNO3(NaCl) | H2O | 重结晶 |
| B | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 溴苯(溴) | H2O | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
5.下列有关物质性质与应用对应关系错误的是( )
| A. | 常温下,浓硫酸能使铝钝化,可用铝制容器贮运浓硫酸 | |
| B. | 二氧化硅熔点很高、硬度很大,可用于制造坩埚 | |
| C. | 氯化铁溶液能腐蚀铜,可用于制作印刷电路板 | |
| D. | 金属钠硬度小、密度小,可用于制造高压钠灯 |
3.现有7瓶失去了标签的液体,已知它们是有机溶剂,可能是①乙醇②乙酸 ③苯④乙酸乙酯 ⑤油脂⑥葡萄糖⑦蔗糖溶液,现通过如下实验步骤来确定试剂中所装的液体名称.
(1)试给它们的试剂瓶重新贴上标签:
A乙醇、B乙酸、C苯、D乙酸乙酯、E油脂、F葡萄糖溶液、G蔗糖溶液;
(2)写出在D中加入NaOH溶液并加热的化学方程式.CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH
(3)已知乙醛发生银镜反应的化学方程式为:
CH3CHO+4[Ag(NH3)2]OH $\stackrel{△}{→}$ (NH4)2CO3+4Ag↓+6NH3↑+2H2O.
试写出葡萄糖发生银镜反应的化学方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{△}{→}$H2O+2Ag↓+3NH3+CH2OH(CHOH)4COONH4.
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体分别依次标号A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
| 分别取少量7种液体于试管中加新制的Cu(OH)2并加热 | 只有B使沉淀溶解,F中产生红色沉淀 |
| 各取C、D、E少量于试管中,加稀NaOH溶液并加热 | 只有C仍有分层现象,且在D的试管中闻到特殊香味 |
A乙醇、B乙酸、C苯、D乙酸乙酯、E油脂、F葡萄糖溶液、G蔗糖溶液;
(2)写出在D中加入NaOH溶液并加热的化学方程式.CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH
(3)已知乙醛发生银镜反应的化学方程式为:
CH3CHO+4[Ag(NH3)2]OH $\stackrel{△}{→}$ (NH4)2CO3+4Ag↓+6NH3↑+2H2O.
试写出葡萄糖发生银镜反应的化学方程式为CH2OH(CHOH)4CHO+2Ag(NH3)2OH$\stackrel{△}{→}$H2O+2Ag↓+3NH3+CH2OH(CHOH)4COONH4.
 .
.
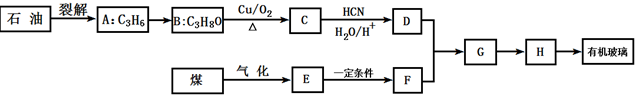
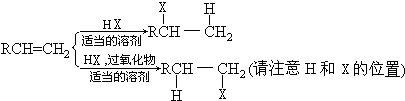
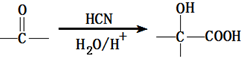
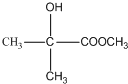 ;有机玻璃的链节是:
;有机玻璃的链节是: ;
;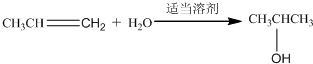 ;
;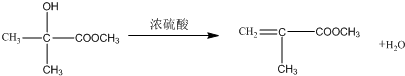 .
.