题目内容
【题目】钠是一种非常活泼、具有广泛应用的金属。
(1)钠的原子结构示意图为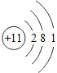 ,钠在反应中容易___电子(填“得到”或“失去”)。
,钠在反应中容易___电子(填“得到”或“失去”)。
(2)金属钠非常活泼,通常保存在________里,以隔绝空气。
(3)汽车安全气囊的气体发生剂NaN3可由金属钠生产。某汽车安全气囊内含NaN3、Fe2O3和NaHCO3等物质。
ⅰ.当汽车发生较严重的碰撞时,引发NaN3分解2NaN3 = 2Na + 3N2,从而为气囊充气。N2的电子式为_________。
ⅱ.产生的Na立即与Fe2O3发生置换反应生成Na2O,化学方程式是________。
ⅲ.NaHCO3是冷却剂,吸收产气过程释放的热量。NaHCO3起冷却作用时发生反应的化学方程式为________。
ⅳ.一个安全气囊通常装有50 g NaN3,其完全分解所释放的N2为_______mol。
(4)工业通过电解NaCl生产金属钠:2NaCl(熔融)![]() 2Na+Cl2,过程如下:
2Na+Cl2,过程如下:

已知:电解时需要将NaCl加热至熔融状态。NaCl的熔点为801℃,为降低能耗,通常加入CaCl2从而把熔点降至约580℃。
①把NaCl固体加热至熔融状态,目的是________。
②电解时,要避免产生的Na与Cl2接触而重新生成NaCl。用电子式表示NaCl的形成过程________。
③粗钠中含有少量杂质Ca,过程Ⅱ除去Ca的化学方程式是________。
④过程Ⅰ中,CaCl2能发生像NaCl那样的电解反应而被消耗。但在过程Ⅰ中CaCl2却不断地被重新生成,原因是________。
【答案】失去 煤油 ![]() 6Na+Fe2O3=3Na2O+2Fe 2NaHCO3
6Na+Fe2O3=3Na2O+2Fe 2NaHCO3![]() Na2CO3+CO2↑+H2O 1.2mol 破坏离子键,产生自由移动的Na+和Cl-
Na2CO3+CO2↑+H2O 1.2mol 破坏离子键,产生自由移动的Na+和Cl- ![]() 2Ca+Na2O2=2CaO+2Na Ca与Na活泼,Ca与Cl2反应生成CaCl2
2Ca+Na2O2=2CaO+2Na Ca与Na活泼,Ca与Cl2反应生成CaCl2
【解析】
(1)根据钠原子的结构示意图最外层电子数分析;
(2)金属钠为活泼金属,能与氧气反应,常保存在煤油中;
(3)i.N2中两个氮原子之间共用叁键;
ii.发生置换反应,利用置换反应特点完成;
iii.利用碳酸氢钠不稳定性进行分析;
iv.根据反应方程式进行计算;
(4)①利用电解质导电条件进行分析;
②NaCl是离子化合物,是由Na+和Cl-组成;
③根据流程进行分析;
④利用金属性强弱进行分析;
(1)根据钠的原子结构示意图,最外层只有1个电子,容易失去1个电子,达到稳定结构;
答案为失去;
(2)金属钠是活泼金属,能与氧气反应,常保存在煤油里,以隔绝空气;
答案:煤油;
(3)i.N2中两个氮原子以叁键结合,且氮原子最外层有5个电子,其电子式为![]() ;
;
答案:![]() ;
;
ii.Na与Fe2O3发生置换反应,根据置换反应特点,Na应将Fe置换出来,即反应方程式为6Na+Fe2O3=3Na2O+2Fe;
答案:6Na+Fe2O3=3Na2O+2Fe;
iii.分解反应为吸热反应,碳酸氢钠不稳定,受热易分解,降低温度,其反应方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
答案:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
iv.根据反应方程式: 解得n(N2)≈1.2mol;
解得n(N2)≈1.2mol;
答案:1.2mol;
(4)①NaCl为电解质,固体不导电,熔融状态下能够导电,破坏离子键,产生自由移动的Na+和Cl-;
答案:破坏离子键,产生自由移动的Na+和Cl-;
②NaCl为离子化合物,是由Na+和Cl-组成,用电子式表示NaCl的形成过程:![]() ;
;
答案:![]() ;
;
③根据过程II,粗钠中加入过氧化钠生成氧化钙和金属钠,因此发生的反应方程式为2Ca+Na2O2=2CaO+2Na;
答案:2Ca+Na2O2=2CaO+2Na;
④过程Ⅰ中,CaCl2被电解成Ca和Cl2,因为Ca比Na活泼,因此Ca与Cl2反应生成CaCl2;
答案:Ca与Na活泼,Ca与Cl2反应生成CaCl2。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案