题目内容
14.已知:氢氧化镁能溶于浓度均为3mol•L-1的①盐酸②NH4Cl溶液③醋酸铵溶液(中性),下列说法正确的是( )| A. | c(NH4+):③>② | |
| B. | Mg(OH)2溶于②的主要原因是由于NH4+水解使溶液显酸性,导致平衡Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)右移 | |
| C. | pH:③>②>① | |
| D. | 将等体积的①和③混合,所得溶液中 c(Cl-)+c(CH3COO-)=c(NH4+)+c(H+) |
分析 A.醋酸根离子促进铵根离子水解,铵根离子水解程度越大,溶液中c(NH4+)越小;
B.NH4++OH-?NH3.H2O,从而促进Mg(OH)2溶解;
C.HCl溶液呈强酸性,氯化铵溶液呈弱酸性,醋酸铵溶液呈中性,据此判断pH大小;
D.等体积等浓度的①和③混合,二者反应生成等物质的量浓度的氯化铵和醋酸,溶液呈酸性,且醋酸电离程度大于铵根离子水解程度,依据电荷守恒分析判断.
解答 解:A.铵根离子水解程度越大,溶液中c(NH4+)越小,醋酸根离子促进铵根离子水解,所以c(NH4+):③<②,故A错误;
B.NH4Cl中含有铵根离子,Mg(OH)2能电离出OH-,NH4++OH-?NH3.H2O,从而促进Mg(OH)2溶解,故B错误;
C.HCl溶液呈强酸性,氯化铵溶液呈弱酸性,醋酸铵溶液呈中性,则三种溶液pH大小顺序是③>②>①,故C正确;
D.等体积等浓度的①和③混合,二者反应生成等物质的量浓度的氯化铵和醋酸,溶液呈酸性,且醋酸电离程度大于铵根离子水解程度,结合电荷守恒所得溶液中 c(Cl-)+c(OH-)+c(CH3COO-)=c(NH4+)+c(H+),故D错误;
故选C.
点评 本题考查了弱电解质的电离和盐类水解、难溶物的溶解平衡等知识点,会正确分析氢氧化镁溶于氯化铵的原因,很多同学往往认为氯化铵水解生成的盐酸溶解氢氧化镁而导致错误,为易错点,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.最近,全国特大“地沟油”案件宣判大快人心.“地沟油”中含有大量的油脂,油脂是多种高级脂肪酸的甘油酯.下列说法不正确的是( )
| A. | 通过适当方法,可将“地沟油”用于生产燃料 | |
| B. | 地沟油有毒,不能回收利用,只能排入下水道 | |
| C. | 地沟油在碱性条件下可水解为甘油和高级脂肪酸盐 | |
| D. | 地沟油可用作化工原料,如生产肥皂等产品 |
5.下列结论错误的是( )
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 微粒半径:K+>Al3+>S2->Cl- | |
| C. | 酸性:H2SO4>CH3COOH>H2CO3>HClO | |
| D. | 金属性:K>Ca>Mg>Be |
2.下列设备工作时,将化学能转化为热能的是( )
| A. | 手机电池 | B. | 硅太阳能电池 | C. | 燃气灶 | D. | 太阳能热水器 |
9.某有机物的结构简式如图,关于该有机物性质的描述不正确的是( )
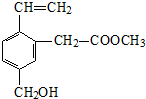
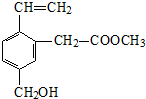
| A. | 能发生水解反应 | B. | 能发生酯化反应 | ||
| C. | 不易溶于水 | D. | 不能使酸性KMnO4溶液褪色 |
19.密闭容器中,A与B反应生成C,已知v(A)、v(B)、v(C)之间有如下关系:3v(A)=2v(B),2v(C)=3v(A),则此反应可表示为( )
| A. | 2A+3B=3C | B. | 3A+2B=2C | C. | 2A+2B=3C | D. | 2A+3B=2C |
3.下列关于有机物的说法正确的是( )
| A. | 乙烯使溴水褪色的反应方程式是:CH2═CH2+Br2→CH3CHBr2 | |
| B. | HOCH2CH2COOH可以发生取代反应 | |
| C. | 煤干馏可得到大量汽油和煤油 | |
| D. | 淀粉(C6H10O5)n和纤维素(C6H10O5)n互为同分异构体,其水解产物都能与新制Cu(OH)2反应生成砖红色沉淀 |
5.金属在生产、生活中的应用十分广泛.
I.某研究性学习小组在探究钠、镁、铝金属性强弱的过程中设计了以下探究性实验方案,请填写下列空白:
实验用品:酒精灯、烧杯、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、2mol•L-1的硫酸
方案如下表:
(1)写出实验a的反应的离子方程式:2Na+2H2O═2Na++2OH-+H2↑
(2)你认为a、b两步实验中出现异常现象的可能原因是:
a.钠表面的煤油没有用滤纸吸干净;
b.镁条表面的氧化膜没有被除去.
(3)下列措施不能提高镁条与硫酸反应产生氢气的速率的是AE
A.改用18mol•L-1的硫酸 B.加入少量硫酸铜
C.改用镁粉 D.升高温度 E.增大压强
Ⅱ.根据以上实验知道,镁比铝活泼,甲同学突发奇想,想设计一个原电池,让镁不腐蚀而铝腐蚀.请你帮他实现这个设想,在下面方框中画出装置图1,并写出负极电极反应式.
Ⅲ.工业上常用铝质容器盛装冷的浓硫酸,为研究铝质材料与热浓硫酸的反应,乙同学进行了以下探究活动:
(1)取铝片6.0g放入15.0mL浓硫酸中,加热,充分反应后收集到气体X.取448ml(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量BaCl2溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中SO2的体积分数为50%.
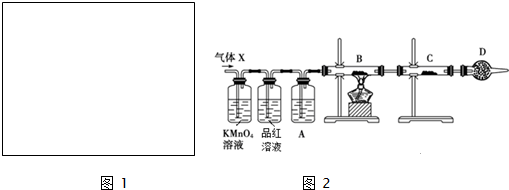
(2)分析上述实验中SO2体积分数的结果,丙同学认为气体X中还可能含量有H2.为此设计了下列探究实验装置(图2中夹持仪器省略).
①A中加入的试剂可能是浓硫酸
②若B中装氧化铜,C中装无水硫酸铜,则可以证明气体X中含有氢气的实验现象是B中固体由黑变红和C中固体由白变蓝.
I.某研究性学习小组在探究钠、镁、铝金属性强弱的过程中设计了以下探究性实验方案,请填写下列空白:
实验用品:酒精灯、烧杯、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、2mol•L-1的硫酸
方案如下表:
| 实验过程 | 预期现象 | 实际观察到的现象 |
| a.取已切去表皮的一小块金属钠,放入盛有水的烧杯中 | 立即剧烈反应 | 开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应 |
| b.向盛有适量水(内含2滴酚酞)的试管中加入一小段镁条 | 有气泡产生,溶液变红色 | 没有相应现象,加热后仍无明显变化 |
| c.向两支盛有3mL 2mol•L-1硫酸的试管中加入大小相同的镁条和铝片 | 镁、铝与硫酸反应产生气泡剧烈程度不同 | 镁与硫酸反应产生气泡速率较快 |
(2)你认为a、b两步实验中出现异常现象的可能原因是:
a.钠表面的煤油没有用滤纸吸干净;
b.镁条表面的氧化膜没有被除去.
(3)下列措施不能提高镁条与硫酸反应产生氢气的速率的是AE
A.改用18mol•L-1的硫酸 B.加入少量硫酸铜
C.改用镁粉 D.升高温度 E.增大压强
Ⅱ.根据以上实验知道,镁比铝活泼,甲同学突发奇想,想设计一个原电池,让镁不腐蚀而铝腐蚀.请你帮他实现这个设想,在下面方框中画出装置图1,并写出负极电极反应式.

Ⅲ.工业上常用铝质容器盛装冷的浓硫酸,为研究铝质材料与热浓硫酸的反应,乙同学进行了以下探究活动:
(1)取铝片6.0g放入15.0mL浓硫酸中,加热,充分反应后收集到气体X.取448ml(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量BaCl2溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中SO2的体积分数为50%.
(2)分析上述实验中SO2体积分数的结果,丙同学认为气体X中还可能含量有H2.为此设计了下列探究实验装置(图2中夹持仪器省略).
①A中加入的试剂可能是浓硫酸
②若B中装氧化铜,C中装无水硫酸铜,则可以证明气体X中含有氢气的实验现象是B中固体由黑变红和C中固体由白变蓝.