题目内容
【题目】(1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
实验序号 | 金属质量/g | 金属状态 | c(H2SO4)/molL-1 | V(H2SO4)/mL | 反应前溶液温度/℃ | 金属消失的时间/s |
1 | 0.10 | 丝 | 0.5 | 50 | 20 | 500 |
2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 50 |
3 | 0.10 | 丝 | 1.0 | 50 | 20 | 125 |
4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 |
对比实验1和3,表明影响化学反应速率的因素是___;此外,该实验表明影响化学反应速率的因素还有___。
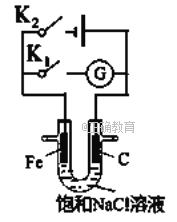
(2)用如图原电池装置可加快铁与稀硫酸反应的速率,其中铜作___(填“负极”或“正极”),铁的电极反应式是___。

(3)举出生活中你熟悉的一种二次电池___。
【答案】反应物浓度 温度、固体表面积 正极 Fe-2e--=Fe2+ 铅酸蓄电池(锂离子电池)
【解析】
略

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目