题目内容
【题目】硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
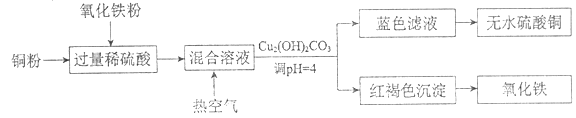
稀硫酸和氧化铁反应的离子方程式是_________;铜和上述反应得到的物质反应的离子方程式是_________;向混合溶液中通入热空气的反应的离子方程式是_________;分离蓝色滤液和红褐色沉淀的实验操作是_________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:
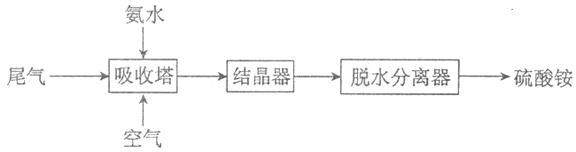
①吸收塔中发生反应的化学方程式是_________。
②检验硫酸铵中的NH4+的离子方程式是_________。
【答案】 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O Fe2O3+6H+=2Fe3++3H2O 2Fe3++Cu=2Fe2++Cu2+ 4Fe2++4H++O2=4Fe2++2H2O 过滤 4NH3·H2O+2SO2+O2=2(NH4)2SO4+2H2O NH4++OH-
CuSO4+SO2↑+2H2O Fe2O3+6H+=2Fe3++3H2O 2Fe3++Cu=2Fe2++Cu2+ 4Fe2++4H++O2=4Fe2++2H2O 过滤 4NH3·H2O+2SO2+O2=2(NH4)2SO4+2H2O NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
【解析】(1)①铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O;故答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
②依据流程转化图分析,铜需要硫酸和氧化铁反应生成的铁离子溶解生成铜离子,再通入空气氧化亚铁离子为铁离子,调节溶液pH使铁离子沉淀除去,得到硫酸铜溶液;加热蒸发浓缩结晶得到硫酸铜晶体;反应的离子方程式为:Fe2O3+6H+═2Fe3++3H2O、2Fe3++Cu═2Fe2++Cu2+(或Fe2O3+Cu+6H+═3H2O+2Fe2++Cu2+);通入空气的作用是氧气氧化亚铁离子为铁离子的反应,反应离子方程式为:4Fe2++4H++O2═4Fe3++2H2O;过滤可以分离蓝色滤液和红褐色沉淀,故答案为:Fe2O3+6H+═2Fe3++3H2O、2Fe3++Cu═2Fe2++Cu2+;4Fe2++4H++O2═4Fe3++2H2O;过滤;
(2)①依据流程图分析,吸收塔中发生反应是二氧化硫、一水合氧气反应生成硫酸铵和水,反应的化学方程式为:4NH3H2O+2SO2+O2═2(NH4)2SO4+2H2O;故答案为:4NH3H2O+2SO2+O2═2(NH4)2SO4+2H2O;
②检验硫酸铵中的NH4+,可以加入氢氧化钠溶液加热转化为氨气检验,离子方程式为NH4++OH-![]() NH3↑+H2O,故答案为:NH4++OH-
NH3↑+H2O,故答案为:NH4++OH-![]() NH3↑+H2O。
NH3↑+H2O。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】(1)某实验小组为了探究影响化学反应速率的因素,进行了稀硫酸与金属铁反应的对照实验,实验数据如下:
实验序号 | 金属质量/g | 金属状态 | c(H2SO4)/molL-1 | V(H2SO4)/mL | 反应前溶液温度/℃ | 金属消失的时间/s |
1 | 0.10 | 丝 | 0.5 | 50 | 20 | 500 |
2 | 0.10 | 粉末 | 0.5 | 50 | 20 | 50 |
3 | 0.10 | 丝 | 1.0 | 50 | 20 | 125 |
4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 |
对比实验1和3,表明影响化学反应速率的因素是___;此外,该实验表明影响化学反应速率的因素还有___。
(2)用如图原电池装置可加快铁与稀硫酸反应的速率,其中铜作___(填“负极”或“正极”),铁的电极反应式是___。

(3)举出生活中你熟悉的一种二次电池___。
【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段反应速率最大___min(填0~1、1~2、2~3、3~4、4~5),原因是____。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率___(设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是(________)
A.蒸馏水
B.KCl溶液
C.KNO3溶液
D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
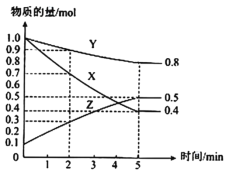
①该反应的化学方程式是___。
②该反应达到平衡状态的标志是___。
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成1molY的同时生成2molZ
③2min内X的转化率为___。