题目内容
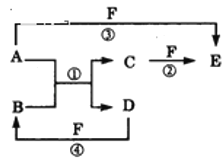
【题目】A、B、C、D、E、F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 其一种单质可吸收紫外线,是地球的保护伞 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
G | G是形成化合物种类最多的元素 |
(1)B元素符号为___,G的元素名称为___,它的一种同位素可测定文物年代,这种同位素的符号是___。
(2)A与C以原子个数比为1:1形成的一种化合物,其所属化合物类型为___(填“离子化合物”或“共价化合物”),包含的化学键有__(填“离子键”、“极性共价键”或“非极性共价键”)。
(3)F常温下可以形成两种用途广泛的氢化物,它们的电子式分别为__和__,并用电子式表示出其最简单气态氢化物的形成过程___。
(4)D在元素周期表中的位置__,D与E相比非金属性较强的是__(填元素名称),请从原子结构的角度解释原因:__。
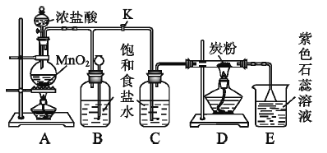
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:___。
【答案】Al 碳 ![]() C 离子化合物 离子键和非极性共价键
C 离子化合物 离子键和非极性共价键 ![]()
![]()
![]() 第三周期第VIA族 氯 氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,即非金属性氯大于硫 4KClO3
第三周期第VIA族 氯 氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,即非金属性氯大于硫 4KClO3![]() KCl+3KClO4
KCl+3KClO4
【解析】
由题干信息,A、B、C、D、E、F、G是周期表中短周期元素,A的一种单质可吸收紫外线,是地球的保护伞,该单质是O3,则A是O元素,B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的,则B为Al元素,C与B同周期,且是所在周期中原子半径最大的(稀有气体除外),则C为Na元素,D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味,则D为S元素,E与D同周期,且在该周期中原子半径最小,则E为Cl元素,F的氢化物和最高价氧化物的水化物反应生成一种离子化合物,则F为N元素,G是形成化合物种类最多的元素,则G是C元素,据此分析解答。
(1)根据上述分析可知,B为Al元素,元素符号为Al,G为C元素,元素名称为碳,![]() C可用于测定文物年代,故答案为:Al;碳;
C可用于测定文物年代,故答案为:Al;碳;![]() C;
C;
(2)O与Na以原子个数比为1:1形成的一种化合物为Na2O2,Na+和O22-形成离子键,O22-中O原子和O原子之间形成非极性共价键,属于离子化合物,故答案为:离子化合物;离子键和非极性共价键;
(3)N在常温下可形成两种用途广泛的氢化物为NH3和N2H4,均属于共价化合物,电子式分别为![]() 和
和![]() ,最简单的气态氢化物为NH3,其形成过程可表示为
,最简单的气态氢化物为NH3,其形成过程可表示为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;![]() ;
;
(4)D为S元素,位于元素周期表的第三周期第ⅥA族,E为Cl元素,由于氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,则非金属性Cl>S,故答案为:第三周期第ⅥA族;氯;氯与硫电子层数相同,氯原子半径小于硫,氯对最外层电子的吸引能力强,所以氯得电子能力强,即非金属性氯大于硫;
(5)根据题干信息可知,KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1,则两种盐为氯化钾和高氯酸钾,反应方程式为4KClO3![]() KCl+3KClO4,故答案为:4KClO3
KCl+3KClO4,故答案为:4KClO3![]() KCl+3KClO4。
KCl+3KClO4。

 阅读快车系列答案
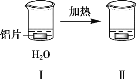
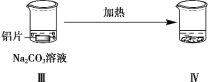
阅读快车系列答案【题目】探究铝片与Na2CO3溶液的反应,下列说法不正确的是( )
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为H2和CO2) |
A.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜
B.Na2CO3溶液中存在平衡:CO32-+H2O![]() HCO3- +OH-
HCO3- +OH-
C.加热和H2逸出对CO32-水解平衡移动方向的影响是相反的
D.推测出现白色浑浊的原因:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-