题目内容
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是( )
A、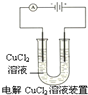 阴极反应式为:2Cl--2e-=Cl2↑,阳极反应式为:Cu2++2e-=Cu |
B、 铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g |
C、 b极为负极,该极的电极反应方程式为O2+2H2O+4e-=4OH- |
D、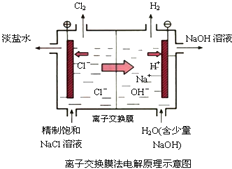 阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.阴极发生还原反应,阳极发生氧化反应;
B.电镀铜电解池中,阳极上金属失电子,阴极上铜离子得电子,根据阴阳极上金属的改变量计算;
C.原电池中负极上失电子发生氧化反应,正极上得电子发生还原反应;
D.气体存在的条件未知.
B.电镀铜电解池中,阳极上金属失电子,阴极上铜离子得电子,根据阴阳极上金属的改变量计算;
C.原电池中负极上失电子发生氧化反应,正极上得电子发生还原反应;
D.气体存在的条件未知.
解答:
解:A.电解时,阴极发生还原反应,电极方程式为Cu2++2e-=Cu,阳极发生氧化反应,电极方程式为2Cl--2e-=Cl2↑,故A错误;
B.该装置中阳极上的电极反应式为 Cu-2e-=Cu2+,当有2mol电子通过时,阳极上溶解64g铜.阴极上发生的电极反应式为Cu2++2e-=Cu,当有2mol电子通过时,阴极上析出64g铜,所以电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g,故B正确;
C.通入氧气的一极为正极,发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,故C错误;
D.不一定为标准状态下,不能确定气体的体积,故D错误.
故选B.
B.该装置中阳极上的电极反应式为 Cu-2e-=Cu2+,当有2mol电子通过时,阳极上溶解64g铜.阴极上发生的电极反应式为Cu2++2e-=Cu,当有2mol电子通过时,阴极上析出64g铜,所以电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g,故B正确;
C.通入氧气的一极为正极,发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,故C错误;
D.不一定为标准状态下,不能确定气体的体积,故D错误.
故选B.
点评:本题综合考查了原电池和电解质,为高考常见题型,侧重于学生的分析能力和计算能力的考查,难度不大,注意燃料电池中,电极反应式的书写要结合电解质溶液的酸碱性确定生成物,易错点为D,注意气体存在的状态.

练习册系列答案
相关题目
已知充分燃烧乙炔(C2H2)气体时生成lmolCO2(g)和0.5molH2O(l)时,并放出akJ的热量,则乙炔燃烧的热化学方程式正确的是( )
| A、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-4akJ?mol-1 | ||
B、C2H2(g)+
| ||
| C、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2akJ?mol-1 | ||
| D、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=akJ?mol-1 |
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
| A、分别在这两种物质的溶液中,加入少量澄清石灰水 |
| B、分别加热这两种固体,将生成的气体通入澄清石灰水中 |
| C、分别在这两种物质的溶液中,加入少量氯化钙溶液 |
| D、分别在这两种物质的等浓度的溶液中,加入少量的稀盐酸 |
已知某无色溶液只由Fe3+、Mg2+、Cu2+、Al3+、NH4+、Cl-、OH-中的几种组成,向此溶液中加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则此溶液中一定大量含有的离子( )
| A、Mg2+、Al3+、NH4+、Cl- |
| B、Mg2+、Al3+、NH4+、Fe3+ |
| C、Mg2+、Cu2+、NH4+、OH- |
| D、Mg2+、Cu2+、NH4+、Cl- |
下列说法错误的是( )
| A、s轨道呈圆形,p轨道呈哑铃形 |
| B、Cr元素在元素周期表的d区 |
| C、焰色反应是因为电子跃迁产生的 |
| D、DNA中的碱基互补配对是通过氢键来实现的 |
下列说法不正确的是( )
| A、最外层电子数为2的元素一定处于ⅡA族 |
| B、Ba(OH)2是离子化合物,既含离子键又含共价键 |
| C、Na的原子半径比Cl的大,但Na+的半径比Cl-的小 |
| D、Cl与Ⅰ同属ⅦA族元素,两者最高价氧化物对应水化物的酸性HClO4>HIO4 |
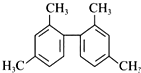 已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是( )
已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是( )| A、该物质所有原子均可共面 |
| B、分子中至少有10个碳原子处于同一平面上 |
| C、分子中至少有11个碳原子处于同一平面上 |
| D、该烃与苯互为同系物 |
下列离子方程式正确的是( )
| A、过量铁屑溶于少量稀硝酸:Fe+4H++NO3-═Fe3++NO↑+2H2O |
| B、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H20+CO2↑ |
| C、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
| D、钢铁发生吸氧腐蚀的正极反应:O2+4e-+4H+═2H2O |
1.1mol氯气跟白磷完全反应生成三氯化磷和五氯化磷,其物质的量比为2:1,则生成物中五氯化磷的物质的量为( )
| A、0.4mol |
| B、0.1mol |
| C、0.2mol |
| D、0.05mol |