题目内容
不能用来鉴别Na2CO3和NaHCO3两种白色固体的实验操作是( )
| A、分别在这两种物质的溶液中,加入少量澄清石灰水 |
| B、分别加热这两种固体,将生成的气体通入澄清石灰水中 |
| C、分别在这两种物质的溶液中,加入少量氯化钙溶液 |
| D、分别在这两种物质的等浓度的溶液中,加入少量的稀盐酸 |
考点:钠的重要化合物,物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题,元素及其化合物
分析:Na2CO3和NaHCO3性质不同:①NaHCO3受热分解,②碳酸钙难溶于水,而碳酸氢钙溶于水,③NaHCO3与盐酸反应剧烈,④都能澄清石灰水反应生成碳酸钙沉淀.
解答:
解:A.Na2CO3和NaHCO3均可与澄清石灰水反应产生沉淀,现象相同,无法鉴别,故A错误;
B.Na2CO3受热不分解,而NaHCO3受热分解,可以鉴别,故B正确;
C.Na2CO3与CaCl2溶液作用产生CaCO3沉淀,而NaHCO3则不与CaCl2溶液反应,无沉淀产生,也可以鉴别,故C正确;
D.向Na2CO3中逐滴加入盐酸时,先无气体产生,当盐酸加入较多时,可产生气体,而向NaHCO3中加入同浓度盐酸,则迅速产生气体,可以通过产生气体的快慢加以鉴别,故D正确.
故选A.
B.Na2CO3受热不分解,而NaHCO3受热分解,可以鉴别,故B正确;
C.Na2CO3与CaCl2溶液作用产生CaCO3沉淀,而NaHCO3则不与CaCl2溶液反应,无沉淀产生,也可以鉴别,故C正确;
D.向Na2CO3中逐滴加入盐酸时,先无气体产生,当盐酸加入较多时,可产生气体,而向NaHCO3中加入同浓度盐酸,则迅速产生气体,可以通过产生气体的快慢加以鉴别,故D正确.
故选A.
点评:本题考查物质的鉴别,题目难度不大,注意碳酸钠和碳酸氢钠的性质的异同,学习中注重相关基础知识的积累.

练习册系列答案
相关题目
下列各组失去标签的溶液,不另加其他试剂(仅利用组内物质间的反应),运用试管和胶头滴管就能区别开来的是( )
| A、FeCl3、NaOH、KSCN、Ba(NO3)2 |
| B、NaCl、Na2CO3、KNO3、HCl |
| C、BaCl2、Na2SO4、NaOH、NaCl |
| D、Na2SO4、BaCl2、K2CO3、KNO3 |
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、M、X、Y组成化合物和Y、Z组成化合物,其等物质的量浓度的水溶液中由水电离出的氢离子浓度相同 |
①在含有FeCl3和BaCl2的酸性混合液中,通入足量SO2气体,有白色沉淀生成,过滤后,向滤液中滴加KSCN溶液,不出现红色,②在氨水和BaCl2的混合液中,通入适量SO2气体,也有白色沉淀生成,由此得出的结论是( )
| A、白色沉淀都是BaSO3 |
| B、①白色沉淀是BaSO3和S,②是BaSO3 |
| C、①白色沉淀是BaSO4,②是BaSO3 |
| D、①白色沉淀是FeSO3,②是BaSO3 |
氯化铁溶液与氢氧化铁胶体的共同点是( )
| A、分散质颗粒直径都在l~100nm之间 |
| B、颜色都呈红褐色 |
| C、一束平行光照射溶液时,从侧面都可以看到一束光束 |
| D、都是分散系 |
下列有关说法正确的是( )
| A、铅蓄电池在放电时,两极质量均增加 | ||
| B、钢铁在中性溶液中主要发生析氢腐蚀 | ||
| C、在室温下能自发进行的反应,其△H一定小于0 | ||
D、0.1mol?L-1 Na2S溶液加水稀释时,
|
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是( )
A、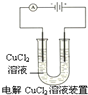 阴极反应式为:2Cl--2e-=Cl2↑,阳极反应式为:Cu2++2e-=Cu |
B、 铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g |
C、 b极为负极,该极的电极反应方程式为O2+2H2O+4e-=4OH- |
D、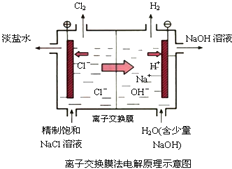 阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2 |
下列电离方程式正确的是( )
| A、Cu(OH)2?Cu2++2OH- |
| B、NaHCO3=Na++H++CO32- |
| C、CH3COOH=CH3COO-+H+ |
| D、H2S?2H++S2- |