题目内容
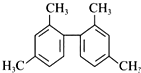 已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是( )
已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是( )| A、该物质所有原子均可共面 |
| B、分子中至少有10个碳原子处于同一平面上 |
| C、分子中至少有11个碳原子处于同一平面上 |
| D、该烃与苯互为同系物 |
考点:常见有机化合物的结构
专题:有机物分子组成通式的应用规律
分析:A、B、C、根据常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,在此基础上进行判断.注意碳碳单键可以绕键轴自由旋转.
D、苯的同系物指含有1个苯环,侧链为烷基.
D、苯的同系物指含有1个苯环,侧链为烷基.
解答:
解:A、甲基与苯环平面结构通过单键相连,甲基的C原子处于苯的H原子位置,所以处于苯环这个平面,两个苯环相连,与苯环相连的碳原子处于另一个苯的H原子位置,也处于另一个苯环这个平面.如图所示(已编号)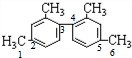 的甲基碳原子、甲基与苯环相连的碳原子、苯环与苯环相连的碳原子,处于一条直线,共有6个原子共线,所以至少有11个碳原子共面,所有原子不可能共面,故A错误;
的甲基碳原子、甲基与苯环相连的碳原子、苯环与苯环相连的碳原子,处于一条直线,共有6个原子共线,所以至少有11个碳原子共面,所有原子不可能共面,故A错误;
B、由A分析可知,分子中至少有11个碳原子处于同一平面上,故B错误;
C、由A分析可知,分子中至少有11个碳原子处于同一平面上,故C正确;
D、该有机物含有2个苯环,不是苯的同系物,故D错误.
故选C.
 的甲基碳原子、甲基与苯环相连的碳原子、苯环与苯环相连的碳原子,处于一条直线,共有6个原子共线,所以至少有11个碳原子共面,所有原子不可能共面,故A错误;
的甲基碳原子、甲基与苯环相连的碳原子、苯环与苯环相连的碳原子,处于一条直线,共有6个原子共线,所以至少有11个碳原子共面,所有原子不可能共面,故A错误;B、由A分析可知,分子中至少有11个碳原子处于同一平面上,故B错误;
C、由A分析可知,分子中至少有11个碳原子处于同一平面上,故C正确;
D、该有机物含有2个苯环,不是苯的同系物,故D错误.
故选C.
点评:本题主要考查有机化合物的结构特点和同系物概念,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.

练习册系列答案
相关题目
下列各组失去标签的溶液,不另加其他试剂(仅利用组内物质间的反应),运用试管和胶头滴管就能区别开来的是( )
| A、FeCl3、NaOH、KSCN、Ba(NO3)2 |
| B、NaCl、Na2CO3、KNO3、HCl |
| C、BaCl2、Na2SO4、NaOH、NaCl |
| D、Na2SO4、BaCl2、K2CO3、KNO3 |
下列有关说法正确的是( )
| A、铅蓄电池在放电时,两极质量均增加 | ||
| B、钢铁在中性溶液中主要发生析氢腐蚀 | ||
| C、在室温下能自发进行的反应,其△H一定小于0 | ||
D、0.1mol?L-1 Na2S溶液加水稀释时,
|
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是( )
A、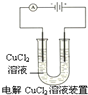 阴极反应式为:2Cl--2e-=Cl2↑,阳极反应式为:Cu2++2e-=Cu |
B、 铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g |
C、 b极为负极,该极的电极反应方程式为O2+2H2O+4e-=4OH- |
D、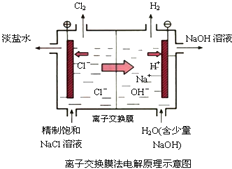 阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1mol?L-1的NaI溶液:K+、H+、SO42-、NO3- |
| B、0.1mol?L-1的NaHCO3溶液:K+、Na+、NO3-、Cl- |
| C、0.1mol?L-1FeCl3溶液:K+、Na+、ClO-、Cl- |
| D、0.1mol?L-1的氨水:Cu2+、Na+、SO42-、NO3- |
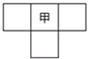 甲、乙、丙、丁为4种短周期元素.甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )
甲、乙、丙、丁为4种短周期元素.甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )| A、甲、乙、丙、丁四种元素的简单气态氢化物中,乙的简单气态氢化物最稳定 |
| B、甲、乙、丙、丁四种元素的常见单质都是无色的 |
| C、由甲元素和丁元素组成的两种常见化合物的分子都是极性分子 |
| D、甲、乙、丙、丁四种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 |
下列电离方程式正确的是( )
| A、Cu(OH)2?Cu2++2OH- |
| B、NaHCO3=Na++H++CO32- |
| C、CH3COOH=CH3COO-+H+ |
| D、H2S?2H++S2- |
在酸性高锰酸钾溶液中加入过氧化钠粉末,溶液褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+.下列判断正确的是( )
| A、Na2O2既是氧化剂,又是还原剂 |
| B、O2是还原产物,Mn2+是氧化产物 |
| C、通常用浓盐酸酸化高锰酸钾溶液 |
| D、标准状况下,产生22.4L O2时反应转移2mol e- |