题目内容
已知某无色溶液只由Fe3+、Mg2+、Cu2+、Al3+、NH4+、Cl-、OH-中的几种组成,向此溶液中加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则此溶液中一定大量含有的离子( )
| A、Mg2+、Al3+、NH4+、Cl- |
| B、Mg2+、Al3+、NH4+、Fe3+ |
| C、Mg2+、Cu2+、NH4+、OH- |
| D、Mg2+、Cu2+、NH4+、Cl- |
考点:离子共存问题,常见离子的检验方法
专题:离子反应专题
分析:无色溶液一定不含Fe3+、Cu2+,向此溶液中加入一种淡黄色粉末状固体时,固体为过氧化钠,加热有刺激性气味的混合气体放出,气体为氨气,则溶液中一定含NH4+;生成的白色沉淀继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则沉淀为氢氧化镁、氢氧化铝,无色气体为氧气,以此来解答.
解答:
解:无色溶液一定不含Fe3+、Cu2+,向此溶液中加入一种淡黄色粉末状固体时,固体为过氧化钠,加热有刺激性气味的混合气体放出,气体为氨气,则溶液中一定含NH4+;生成的白色沉淀继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则沉淀为氢氧化镁、氢氧化铝,无色气体为氧气,则溶液含Mg2+、Al3+、NH4+,与OH-不能共存,又溶液为电中性,则一定含阴离子为Cl-,
故选A.
故选A.
点评:本题考查离子的共存及推断,为高频考点,把握常见离子的颜色、离子之间的反应为解答的关键,注意过氧化钠与水反应生成碱和气体,题目难度不大.

练习册系列答案
相关题目
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、M、X、Y组成化合物和Y、Z组成化合物,其等物质的量浓度的水溶液中由水电离出的氢离子浓度相同 |
氯化铁溶液与氢氧化铁胶体的共同点是( )
| A、分散质颗粒直径都在l~100nm之间 |
| B、颜色都呈红褐色 |
| C、一束平行光照射溶液时,从侧面都可以看到一束光束 |
| D、都是分散系 |
下列有关说法正确的是( )
| A、铅蓄电池在放电时,两极质量均增加 | ||
| B、钢铁在中性溶液中主要发生析氢腐蚀 | ||
| C、在室温下能自发进行的反应,其△H一定小于0 | ||
D、0.1mol?L-1 Na2S溶液加水稀释时,
|
下列叙述与对应图式正确的是( )
A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强
| |||||||||||||||||||||||||||||||||||
B、图甲表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2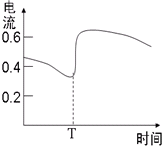 | |||||||||||||||||||||||||||||||||||
C、图乙表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变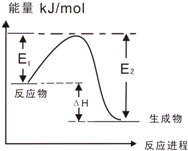 | |||||||||||||||||||||||||||||||||||
| D、表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ/mol |
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是( )
A、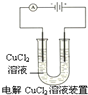 阴极反应式为:2Cl--2e-=Cl2↑,阳极反应式为:Cu2++2e-=Cu |
B、 铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2mol电子转移,此时铜片和铁制品的质量差为128g |
C、 b极为负极,该极的电极反应方程式为O2+2H2O+4e-=4OH- |
D、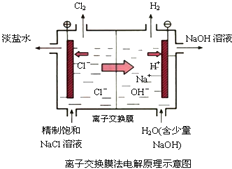 阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2 |
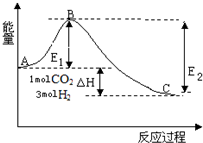 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.