题目内容
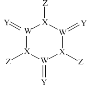
【题目】科学家研制出了一种漂白效率极高的新型漂白剂(结构如图所示),其中W、X、Y、Z均为短周期元素且原子序数依次增大。常温下,0.1 mol/L Z的氢化物的水溶液中c(H+ )=0.1 mol/L,且Z与Y位于不同周期。下列叙述正确的是
A.原子半径:W> X> YB.氢化物的沸点:Y >X> Z> W
C.X的氧化物的水化物是强酸D.Y的单质均具有杀菌消毒作用
【答案】A
【解析】
由新型漂白剂的结构可知,W形成的价键数为4,X形成的价键数为3,Y形成的价键数为2,Z形成的价键数为1;W、X、Y、Z均为短周期元素且原子序数依次增大,常温下,0.1mol/LZ的氢化物的水溶液c(H+ )=0.1 mol/L,Z的氢化物为强酸,则Z为Cl;Z与Y位于不同周期,则Y为O元素、W为C元素、X为N元素,据此分析解题。
A. C、N、O为同周期主族元素,核电荷数越大,原子半径越小,C、N、O三种元素的原子半径由大到小的顺序为C>N>O,即W>X>Y,故A正确;
B. H2O常温下为液体,NH3和H2O分子间存在氢键,四种元素简单氢化物的沸点由高到低的顺序为H2O>NH3>HCl>CH4,但C的氢化物包括多碳的烃,常温下有固体,有液体,即碳的氢化物沸点也可能比H2O高,故B错误;
C. N的最高价氧化物的水化物HNO3是强酸,而+3价N的氧化物水化物HNO2是弱酸,故C错误;
D. Y的单质有氧气和臭氧,O3具有强氧化性,具有杀菌消毒作用,而氧气不能杀菌消毒,故D错误;
答案选A。

练习册系列答案
相关题目