题目内容
【题目】下列实验操作和现象能得出正确结论的是![]()
![]()
选项 | 实验操作 | 现象 | 结论 |
A | 向淀粉 | 溶液变蓝 | 达到滴定终点 |
B | 将 | 品红溶液颜色不褪色 |
|
C | 向浓度均为 | 先产生红褐色沉淀 | 相同温度下, |
D | 向饱和纯碱溶液中通入 | 产生白色沉淀 | 小苏打属于难溶物 |
A.AB.BC.CD.D
【答案】C
【解析】
A.开始滴加![]() 溶液时即生成
溶液时即生成![]() ,溶液变蓝,不能准确判定滴定终点,故A错误;
,溶液变蓝,不能准确判定滴定终点,故A错误;
B.![]() 和
和![]() 在水溶液中以物质的量之比
在水溶液中以物质的量之比![]() 反应生成
反应生成![]() 和HCl,生成物均无漂白性,故B错误;
和HCl,生成物均无漂白性,故B错误;
C.![]() 中
中![]() 与
与![]() 数目之比大于
数目之比大于![]() 中
中![]() 与
与![]() 数目之比,在金属阳离子浓度相等的混合溶液中先生成
数目之比,在金属阳离子浓度相等的混合溶液中先生成![]() 沉淀,说明相同温度下,
沉淀,说明相同温度下,![]() ,故C正确;
,故C正确;
D.纯碱易溶于水,小苏打可溶于水,故D错误。
故选C。

【题目】已知:H2(g)+I2(g) ![]() 2HI(g) H=-149kJ/mol。在甲、乙两个体积相同的密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。
2HI(g) H=-149kJ/mol。在甲、乙两个体积相同的密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。
起始 浓度 | c(H2)(mol/L) | c(I2)(mol/L) | c(HI)/(mol/L) |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
甲中反应达到平衡时,测得c(H2)=0.008 mol/L下列判断正确的是( )
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
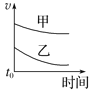
【题目】下列表格中的各种情况,可以用对应选项中的图像表示的是
选项 | 反应 | 甲 | 乙 |
A | 外形、大小相近的金属和水反应 | Na | K |
B | 4mL0.01mol·L-1 KMnO4溶液分别和不同浓度的2mLH2C2O4(草酸)溶液反应 | 0.1mol·L-1的H2C2O4溶液 | 0.2mol·L-1的H2C2O4溶液 |
C | 5mL0.1mol·L-1Na2S2O3溶液和5mL0.1mol·L-1H2SO4溶液反应 | 热水 | 冷水 |
D | 5mL4%的过氧化氢溶液分解放出O2 | 无MnO2粉末 | 加MnO2粉末 |
A.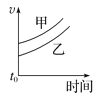 B.
B.
C. D.
D.