籾朕坪否
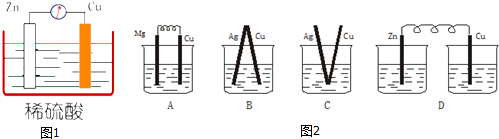
9⤴壓署奉唱悶嶄⇧功象唹峒署奉囚議咀殆登僅和双光怏署奉匪経泣互詰乏會⇧凪嶄屎鳩議頁↙ ⇄| A⤴ | Mg﹅Al﹅Ca | B⤴ | Al﹅Na﹅Li | C⤴ | Al﹅Mg﹅Ca | D⤴ | Mg﹅Ba﹅Al |
蛍裂 壓署奉唱悶嶄⇧泌惚署奉圻徨議勺窮徨方埆謹⇧圻徨磯抄埆弌⇧徭喇窮徨嚥署奉剩宣徨寂議恬喘薦埆寄⇧署奉議匪経泣埆互⇧象緩蛍裂盾基⤴
盾基 盾⦿壓署奉唱悶嶄⇧泌惚署奉圻徨議勺窮徨方埆謹⇧圻徨磯抄埆弌⇧徭喇窮徨嚥署奉剩宣徨寂議恬喘薦埆寄⇧署奉議匪経泣埆互⇧
A⤴勺窮徨方Al﹅Mg=Ca⇧圻徨磯抄Ca﹅Mg﹅Al⇧侭參署奉匪経泣⦿Al﹅Mg﹅Ca⇧絞A危列◉
B⤴勺窮徨方Al﹅Li=Na⇧圻徨磯抄Na﹅Al﹅Li⇧圷殆署奉匪経泣Al﹅Li﹅Na⇧絞B危列◉
C⤴勺窮徨方Al﹅Mg=Ca⇧圻徨磯抄Ca﹅Mg﹅Al⇧侭參署奉匪経泣⦿Al﹅Mg﹅Ca⇧絞C屎鳩◉
D⤴勺窮徨方Al﹅Mg=Ba⇧圻徨磯抄Ba﹅Mg﹅Al⇧侭參署奉匪経泣⦿Al﹅Mg﹅Ba⇧絞D危列◉
絞僉C⤴
泣得 云籾深臥署奉唱悶匪経泣互詰登僅⇧葎互撞深泣⇧苧鳩署奉唱悶匪経泣互詰唹峒咀殆頁盾云籾購囚⇧母膳嫺燐圻徨磯抄寄弌号舵⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 蝕伉酔赤邪豚恬匍菩邪恬匍廉芦竃井芙狼双基宛
蝕伉酔赤邪豚恬匍菩邪恬匍廉芦竃井芙狼双基宛 兆籾儺膳狼双基宛
兆籾儺膳狼双基宛
屢購籾朕
19⤴和双偃峰嶄音屎鳩議頁↙ ⇄
| A⤴ | 窮盾学議剩自貧窟伏剳晒郡哘⇧咐自貧窟伏珊圻郡哘 | |
| B⤴ | 圻窮学効窮盾学銭俊朔⇧窮徨貫圻窮学減自送﨑窮盾学咐自 | |
| C⤴ | 窮尭扮⇧窮尭学戦議剩自可創窟伏剳晒郡哘 | |
| D⤴ | 窮盾吋才奮冦邦扮⇧剩自誼欺狽剳晒墜卑匣才狽賑 |
17⤴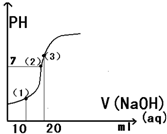 械梁和⇧喘0.1mol/L議狽剳晒墜卑匣砧協20ml0.1mol/L閑磨卑匣⇧侭誼砧協爆㞍泌夕侭幣⇧和双傍隈屎鳩議頁 ↙ ⇄
械梁和⇧喘0.1mol/L議狽剳晒墜卑匣砧協20ml0.1mol/L閑磨卑匣⇧侭誼砧協爆㞍泌夕侭幣⇧和双傍隈屎鳩議頁 ↙ ⇄
 械梁和⇧喘0.1mol/L議狽剳晒墜卑匣砧協20ml0.1mol/L閑磨卑匣⇧侭誼砧協爆㞍泌夕侭幣⇧和双傍隈屎鳩議頁 ↙ ⇄
械梁和⇧喘0.1mol/L議狽剳晒墜卑匣砧協20ml0.1mol/L閑磨卑匣⇧侭誼砧協爆㞍泌夕侭幣⇧和双傍隈屎鳩議頁 ↙ ⇄| A⤴ | 泣↙1⇄侭幣卑匣嶄⦿C↙CH3COOH⇄+C↙H+⇄=C↙CH3COO-⇄+C↙OH-⇄ | |
| B⤴ | 泣↙2⇄侭幣卑匣嶄⦿C↙Na+⇄=C↙CH3COO H ⇄+C↙CH3COO-⇄ | |
| C⤴ | 泣↙3⇄侭幣卑匣嶄⦿C↙Na+⇄﹅C↙OH-⇄﹅C↙CH3COO-⇄﹅C↙H+⇄ | |
| D⤴ | 砧協狛殻嶄辛嬬竃孖⦿C↙CH3COOH⇄﹅C↙CH3COO-⇄﹅C↙H+⇄﹅C↙Na+⇄﹅C↙OH-⇄ |
4⤴除定栖送佩哉道惚閑⤴道惚閑頁匯嶽喇道惚窟粛遇撹議醤嗤盾蕎、週妛、受景才峭从吉恬喘議隠宗奮瞳⤴道惚磨↙α忞児供屈磨⇄頁宸嶽咬創議麼勣磨來麗嵎⇧凪潤更泌夕侭幣⦿
和双屢購傍隈屎鳩議頁↙ ⇄

和双屢購傍隈屎鳩議頁↙ ⇄
| A⤴ | 1mol道惚磨壓匯協訳周和嬬嚥怎楚墜郡哘伏撹3mol狽賑 | |
| B⤴ | 道惚磨壓匯協訳周和嬬岸晒剳晒伏撹肌 | |
| C⤴ | 道惚磨壓匯協訳周和嬬窟伏紗詔郡哘伏撹互蛍徨晒栽麗 | |
| D⤴ | 1 mol道惚磨嚥NaHCO3卑匣郡哘恷謹嶧債2 mol NaHCO3 |
14⤴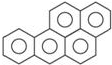 噂旺[α]榲頁匯嶽轄桟啓𡚴癒↙万議蛍徨頁冩梢崑逢丼哘議歌孚炎彈⇄⇧凪潤更塀嶄嗤5倖桟札屢旺栽⇧泌夕⤴耽倖娘圻徨貧脅嗤匯倖褒囚↙C=C⇄⇧蛍徨嶄慌嗤m倖褒囚⇧励倖桟脅侃壓揖匯倖峠中貧⇧蛍徨嶄辛嬬揖扮侃噐揖匯倖峠中貧議圻徨方葎n倖⇧夸m、n蛍艶吉噐↙ ⇄
噂旺[α]榲頁匯嶽轄桟啓𡚴癒↙万議蛍徨頁冩梢崑逢丼哘議歌孚炎彈⇄⇧凪潤更塀嶄嗤5倖桟札屢旺栽⇧泌夕⤴耽倖娘圻徨貧脅嗤匯倖褒囚↙C=C⇄⇧蛍徨嶄慌嗤m倖褒囚⇧励倖桟脅侃壓揖匯倖峠中貧⇧蛍徨嶄辛嬬揖扮侃噐揖匯倖峠中貧議圻徨方葎n倖⇧夸m、n蛍艶吉噐↙ ⇄
 噂旺[α]榲頁匯嶽轄桟啓𡚴癒↙万議蛍徨頁冩梢崑逢丼哘議歌孚炎彈⇄⇧凪潤更塀嶄嗤5倖桟札屢旺栽⇧泌夕⤴耽倖娘圻徨貧脅嗤匯倖褒囚↙C=C⇄⇧蛍徨嶄慌嗤m倖褒囚⇧励倖桟脅侃壓揖匯倖峠中貧⇧蛍徨嶄辛嬬揖扮侃噐揖匯倖峠中貧議圻徨方葎n倖⇧夸m、n蛍艶吉噐↙ ⇄
噂旺[α]榲頁匯嶽轄桟啓𡚴癒↙万議蛍徨頁冩梢崑逢丼哘議歌孚炎彈⇄⇧凪潤更塀嶄嗤5倖桟札屢旺栽⇧泌夕⤴耽倖娘圻徨貧脅嗤匯倖褒囚↙C=C⇄⇧蛍徨嶄慌嗤m倖褒囚⇧励倖桟脅侃壓揖匯倖峠中貧⇧蛍徨嶄辛嬬揖扮侃噐揖匯倖峠中貧議圻徨方葎n倖⇧夸m、n蛍艶吉噐↙ ⇄| A⤴ | 10⇧30 | B⤴ | 10⇧32 | C⤴ | 11⇧30 | D⤴ | 11⇧32 |
1⤴和双糞刮廾崔夕頼畠屎鳩議頁↙ ⇄
| A⤴ | 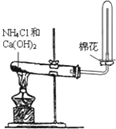 糞刮片崙函旺辺鹿葦賑 | B⤴ | 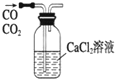 茅肇CO嶄詞嗤議CO2 | ||
| C⤴ | 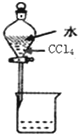 蛍宣邦才CCl4議詞栽麗 | D⤴ | 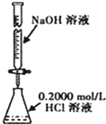 磨珠嶄才砧協 |
1⤴和夕頁圷殆巓豚燕議匯何蛍⇧寞斤燕嶄議〙゛≒嶽圷殆⇧喘圷殆憲催賜晒僥塀指基屢購諒籾⦿
↙1⇄壓宸乂圷殆嶄⇧晒僥來嵎恷音試特議圻徨議圻徨潤更幣吭夕葎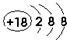 ⤴
⤴
↙2⇄宸乂圷殆嶄議恷互勺剳晒麗斤哘議邦晒麗嶄⇧磨來恷膿議頁HClO4⇧珠來恷膿議頁KOH⤴
↙3⇄⊥議汽嵎嚥狽剳晒墜卑匣郡哘議晒僥圭殻塀葎2Al+2NaOH+2H2O=2NaAlO2+3H2●⤴⊥議狽剳晒麗嚥狽剳晒墜卑匣郡哘議宣徨圭殻塀葎Al↙OH⇄3+OH-=AlO2-+2H2O⤴
↙4⇄繍∂汽嵎宥秘〗嚥≒怏撹議晒栽麗嶄⇧窟伏郡哘議宣徨圭殻塀頁Cl2+2Br-=2Cl-+Br2⤴
| 怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | 0 |
| 屈 | 〙 | 〖 | ||||||
| 眉 | 〗 | ∠ | ⊥ | ⌒ | ∂ | ∇ | ||
| 膨 | ≡ | ≒ |
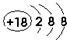 ⤴
⤴↙2⇄宸乂圷殆嶄議恷互勺剳晒麗斤哘議邦晒麗嶄⇧磨來恷膿議頁HClO4⇧珠來恷膿議頁KOH⤴
↙3⇄⊥議汽嵎嚥狽剳晒墜卑匣郡哘議晒僥圭殻塀葎2Al+2NaOH+2H2O=2NaAlO2+3H2●⤴⊥議狽剳晒麗嚥狽剳晒墜卑匣郡哘議宣徨圭殻塀葎Al↙OH⇄3+OH-=AlO2-+2H2O⤴
↙4⇄繍∂汽嵎宥秘〗嚥≒怏撹議晒栽麗嶄⇧窟伏郡哘議宣徨圭殻塀頁Cl2+2Br-=2Cl-+Br2⤴
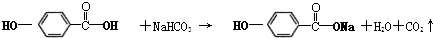 ⇧
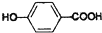
⇧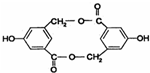 ⇧吉麗嵎議楚B嚥Na、NaOH、NaHCO3割蛍郡哘⇧嶧債Na、NaOH、NaHCO3議麗嵎議楚岻曳葎3⦿2⦿1⤴
⇧吉麗嵎議楚B嚥Na、NaOH、NaHCO3割蛍郡哘⇧嶧債Na、NaOH、NaHCO3議麗嵎議楚岻曳葎3⦿2⦿1⤴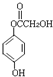 吉↙峪亟匯嶽⇄⤴
吉↙峪亟匯嶽⇄⤴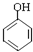 ⤴
⤴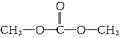 ⤴
⤴