题目内容
15.22gCO2跟多少g水的分子数相等( )| A. | 9g | B. | 18g | C. | 22g | D. | 44g |
分析 根据n=$\frac{m}{M}$计算22g CO2的物质的量,水与22g CO2所含分子数相等,则二者物质的量相等,再根据m=nM计算水的质量.
解答 解:22g CO2的物质的量=$\frac{22g}{44g/mol}$=0.5mol,水与22g CO2所含分子数相等,则水的物质的量为0.5mol,故水的质量=0.5mol×18g/mol=9g,
故选A.
点评 本题考查常用化学计量的有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
6.下列有关维生素C的说法中正确的是( )
| A. | 维生素C难溶于水 | |
| B. | 食品中添加维生素C不利于身体健康 | |
| C. | 维生素C具有还原性 | |
| D. | 含维生素C的食物不宜在高温下烹调 |
3.除去Na2CO3 固体中混有少量NaHCO3的最佳方法是( )
| A. | 加入适量盐酸 | B. | 加入NaOH溶液 | ||
| C. | 置于坩埚中加热 | D. | 配成溶液后通入CO2 |
7.水污染主要来自:①工业生产中废渣、废液的任意排放②雨水和土壤接触③农业生产中农药、化肥的过量使用④城市生活污水的任意排放( )
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
4.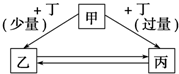 甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
 甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )
甲、乙、丙、丁均为中学化学中常见的物质,它们之间存在如图所示的转化关系(部分产物略去),甲不可能是( )| A. | NaOH溶液 | B. | Fe | C. | Al2O3 | D. | C |
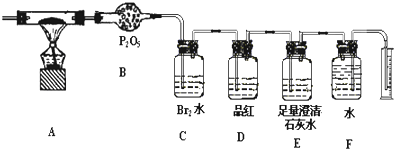
 如图是常见原电池装置,电流表G发生偏转:
如图是常见原电池装置,电流表G发生偏转: