题目内容
【题目】工业上冶炼钼的化学原理为:
①2MoS2+7O2![]() 2MoO3+4SO2
2MoO3+4SO2
②MoO3+2NH3·H2O=(NH4)2MoO4+H2O
③(NH4)2MoO4+2HCl=H2MoO4↓+2NH4Cl
④H2MoO4![]() MoO3+H2O
MoO3+H2O
⑤用还原剂将MoO3还原成金属钼。则下列说法中正确的是
A.MoS2煅烧产生的尾气可以直接排到空气中
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
【答案】D
【解析】
A. 从反应①看,MoS2煅烧后的产物中有SO2,它是大气污染物,因此尾气不能直接排入空气中,故A错误;
B. 所谓碱性氧化性,是跟酸反应生成盐和水的氧化物,但从反应②可看出,MoO3和碱反应生成盐和水,因此MoO3应该是酸性氧化物,又从反应③看,MoO3是H2MoO4的酸酐,因此不可能是碱性氧化物,故B错误;
C. 由③可知,强酸制弱酸,所以H2MoO4的酸性比盐酸弱,无法确定是不是弱酸,故C错误;
D. 因为MoO3中钼元素显+6价,1molMoO3能得到6mol电子,而1molH2、CO、Al分别失去的电子数为2mol、2mol、3mol,根据电子守恒规律可知所消耗还原剂的物质的量之比为3:3:2,故D正确;
答案选D。

练习册系列答案
相关题目
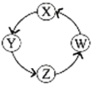
【题目】X、Y、Z、W 四种物质间的转化关系如图所示 ,下列转化不能一步实现的是( )
序号 | X | Y | Z | W | 转化关系 |
A | FeCl3 | FeCl2 | Fe(OH)2 | Fe(OH)3 |
|
B | Na | NaOH | Na2CO3 | NaCl | |
C | Cl2 | Ca(ClO)2 | HClO | HCl | |
D | H2S | S | SO3 | H2SO4 |
A.AB.BC.CD.D