题目内容
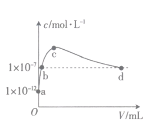
【题目】常温下,将SO2通入2L0.01mol·L-1的某一元碱MOH溶液中,溶液中水电离出的OH-的浓度(c)与通入的SO2的体积(V)关系如图所示(不考虑+4价的S被氧化),下列叙述不正确的是
A.MOH为一元强碱
B.b点溶液中:c(H+)=1×10-7mol·L-1
C.c点溶液中:c(M+)=2[c(SO32-))+c(HSO3-)+c(H2SO3)]
D.d点溶液中:c(M+)=2c(SO32-)+c(HSO3-)
【答案】B
【解析】
将SO2通入2L0.01mol·L-1的某一元碱MOH溶液中,先发生SO2+2MOH=M2SO3+H2O,再发生M2SO3+SO2+H2O=2MHSO3;当溶液中溶质只有M2SO3时,只有SO32-的水解促进水的电离,此时水的电离程度达到最大,即c点。
A.未通入SO2时水电离出的c(OH-)=1×10-12mol/L,水电离出的氢离子浓度和氢氧根浓度相同,所以水电离出的c(H+)=1×10-12mol/L,则溶液中c(OH-)=1×10-2mol/L,说明MOH完全电离,为一元强碱,故A正确;
B.根据分析可知b点溶液中的溶质为M2SO3和未反应的MOH,溶液呈碱性,所以溶液中c(H+)<1×10-7mol·L-1,故B错误;
C.根据分析可知c点溶液中的溶质只有M2SO3,根据物料守恒可知c(M+)=2[c(SO32-))+c(HSO3-)+c(H2SO3)],故C正确;
D.根据分析结合图像可知d点溶液中的溶质为M2SO3和MHSO3以及H2SO3,且水电离出的c(OH-)=1×10-7mol/L,说明此时溶液呈中性,即c(OH-)= c(H+),结合溶液中存在的电荷守恒c(H+)+c(M+)=2c(SO32-)+c(HSO3-)+ c(OH-)可得c(M+)=2c(SO32-)+c(HSO3-),故D正确;
故答案为B。

【题目】某物质 A 是 B(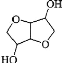 )的同分异构体,7.30 g 的 A 与足量饱和碳酸氢钠可释放出 2.24L 二氧化碳(标准状况),A 的可能结构共有( )种(不考虑立体异构)
)的同分异构体,7.30 g 的 A 与足量饱和碳酸氢钠可释放出 2.24L 二氧化碳(标准状况),A 的可能结构共有( )种(不考虑立体异构)
A.8B.9C.10D.11
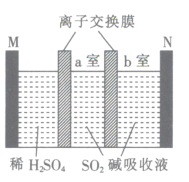
【题目】乙二醛(OHC-CHO)是一种重要的精细化工产品。某小组利用乙醛液相硝酸氧化法制备乙二醛并测定乙二醛纯度,装置如图所示:
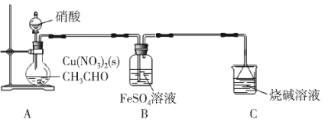
已知:①NO+FeSO4=FeSO4·NO(棕色)。
②几种有机物的部分性质如表所示:
乙醛 | 乙二醛 | 乙二酸 | 乙酸 | |
沸点/℃ | 20.8 | 50.5 | 109 | 117.9 |
溶解性 | 与水、有机溶剂互溶 | 溶于水、乙醇等 | 溶于水和有机溶剂 | 与水、乙醇互溶 |
密度/gcm-3 | 0.78 | 1.27 | 1.90 | 1.05 |
相对分子质量 | 44 | 58 | 90 | 60 |
实验步骤:
①取20 mL乙醛装于烧瓶,加入2 g Cu(NO3)2粉末作催化剂,向烧瓶中缓慢滴加2 mol·L-1硝酸至乙醛完全反应为止;
②提纯产品,最终得到10.0 mL产品。
请回答下列问题:
(1)盛装硝酸的仪器名称是___________。
(2)实验中,观察到装置B中溶液变为棕色,制备乙二醛的化学方程式为________________。
(3)向烧瓶中滴加硝酸要“缓慢”,其目的是___________;判断烧瓶中制备乙二醛的反应已完成的标志是___________。
(4)分离提纯产品,宜选择下列装置___________(填字母)。
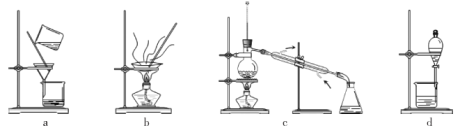
(5)根据上述实验数据,该实验中乙二醛的产率约为___________(填字母)。
a.56.5% b.61.8% c.67.9% d.72.6%
(6)实验室可用酸性KMnO4溶液测定乙二醛的纯度,发生反应的离子方程式为:18H++6MnO4-+5C2H2O2→10CO2↑+6Mn2++14H2O。实验步骤如下:取V mL产品,加蒸馏水稀释至250 mL,量取25.00 mL稀释后的溶液于锥形瓶,滴加5.00 mL稀硫酸,用c mol·L-1 KMnO4溶液,三次平行实验消耗KMnO4溶液体积如下:
实验 | Ⅰ | Ⅱ | Ⅲ |
V[KmnO4(aq)]/mL | 20.05 | 22.40 | 19.95 |
滴定终点的标志是___________;该产品纯度为___________g·mL-1(用含V和c的代数式表示)。