题目内容
【题目】维生素C是一种水溶性维生素(其水溶液呈酸性),结构如图所示。人体缺乏维生素C易得坏血症,所以维生素C又称抗坏血酸。下列关于维生素C的叙述正确的是
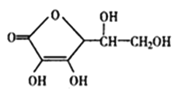
A.维生素C化学式为C6H7O6
B.维生素C能与溴水或酸性高锰酸钾发生加成反应而使其褪色
C.维生素C分子中含有羧基
D.维生素C可发生酯化反应
【答案】D
【解析】
A. 由维生素C的分子结构可知其化学式为C6H8O6,烃的含氧衍生物中的H原子数一定是偶数,A不正确;
B. 维生素C分子中含有碳碳双键和羟基,其具有较强的还原性,故其能与酸性高锰酸钾发生氧化反应而使其褪色,其不能与酸性高锰酸钾发生加成反应,B不正确;
C. 维生素C分子中不含有羧基,C不正确;
D. 维生素C分子中有羟基,故其可发生酯化反应,D正确。
本题选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验方案不能达到相应目的的是
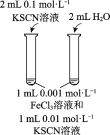
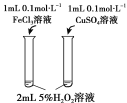
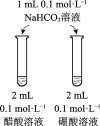
A | B | C | D | |
目的 | 比较碳酸根与碳酸氢根水解程度 | 研究浓度对化学平衡的影响 | 比较不同催化剂对化学反应速率的影响 | 比较碳酸、醋酸和硼酸的酸性强弱 |
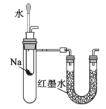
实验方案 |
|
|
|
|
A. AB. BC. CD. D
【题目】设反应①Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。测得在不同温度下,K1、K2值如下:
FeO(s)+H2(g)的平衡常数为K2。测得在不同温度下,K1、K2值如下:
温度/℃ | K1 | K2 |
500 | 1.00 | 3.15 |
700 | 1.47 | 2.26 |
900 | 2.40 | 1.60 |
(1)若500 ℃时进行反应①,CO2的转化率为_______________。
(2)900 ℃时进行反应③H2(g)+CO2(g)![]() H2O(g)+CO(g),其平衡常数K3=______________。
H2O(g)+CO(g),其平衡常数K3=______________。
(3)反应②的焓变ΔH____________(填“>”、“<”或“=”)0。
(4)700 ℃时反应②达到化学平衡,要使该平衡向正反应方向移动,当其他条件不变时,可采取的措施有___________________________________。
A.缩小容器容积 B.加入更多的水蒸气
C.升高温度至900 ℃ D.使用合适的催化剂
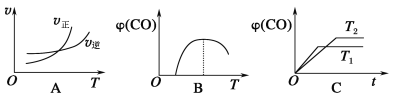
(5)下列图像符合反应①的是________________________。