��Ŀ����
2�����ɽ����ĵ��ʼ�������ܶ��д����ܣ��Ȼ�ͭ���Ȼ���ͭ���������л��ϳɴ�����ʵ���������������ͭ������ֻ��Fe����Ӧ���Ʊ�ͭ���Ȼ�����������£�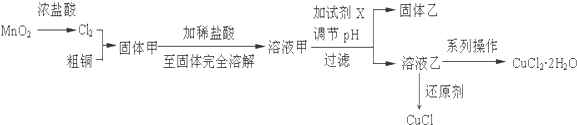
�������ϣ�
�Ȼ���ͭ����ɫ����ˮ���ڸ���������ȶ����ܳ����ױ�������ɫ������ˮ��Ѹ��ˮ����������ͭˮ������ʺ�ɫ��
�Ȼ�ͭ����ˮ��Һ�нᾧʱ����26��42��õ���ˮ���15�����µõ���ˮ���15��25.7��õ���ˮ���42�����ϵõ�һˮ���100��õ���ˮ�
��1��������ͼ��ʾ��ʵ��������ҩƷ�Ʊ���������������������ͭ��Ӧ������̨������ʡ�ԣ���
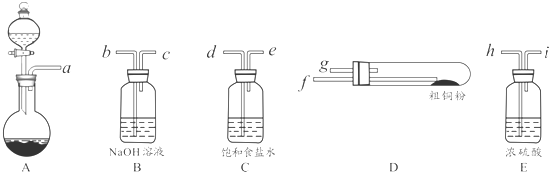
�ٰ������������Ӹ������ӿ�˳���ǣ�a��d��e��h��i��f��g��b��
�ڱ���װ��������������Ҫ���ȣ����ȵ�˳��Ϊ��A��D����������Ŀ�����ų���������ֹͭ������������
��2���������̣�
�ٹ������Ҫ��ϡ�����ܽ⣬�������������Ȼ�ͭ���Ȼ���ˮ�⣻
����Һ�ɼ��Լ�X���ڵ���pH�Գ�ȥ���ʣ�X��ѡ�������Լ��еģ�����ţ�c��
a��NaOH b�� NH3•H2O c��CuO d��CuSO4
�������Һ�ҵ�����CuCl2•2H2O�����ϵ�в�������Ϊ�����������ᡢ����Ũ������ȴ��26��42��ᾧ�����ˡ�ϴ�ӡ����
��3������Һ���м����ʵ��Ļ�ԭ������SO2��N2H4��SnCl2�ȣ������ȵõ�CuCl������д��������Һ����N2H4����������Ϊ�����壩�����ӷ���ʽ��4Cu2++4Cl-+N2H4$\frac{\underline{\;\;��\;\;}}{\;}$4CuCl��+N2��+4H+���˷�Ӧֻ���ȵ�ԭ������ά�ַ�Ӧ�������¶ȹ�����������ͭˮ���
��4������ʼȡ100g ��ͭ96%�Ĵ�ͭ������Cl2��Ӧ������������ֻ�Ʊ�CuCl2•2H2O�����յõ������Ʒ277g�����Ʊ�CuCl2•2H2O�IJ���108%������ȷ��1%���������ִ��������Ҫԭ���ڵ�����ҺpHʱ������CuO��Ӧ������CuCl2��ʹ��Ʒ�������ӣ�
���� ��ͭ������ֻ��Fe����������Ӧ�õ�����������Ȼ�ͭ���Ȼ������������ܽ⣬�����Ȼ�ͭ���Ȼ���ˮ�⣬��Һ���м���X������ҺpH���õ���Һ�ң�����ϵ�в����õ�CuCl2•2H2O������Һ��ΪCuCl2��Һ�������pHĿ����ʹ��Һ��������ת��ΪFe��OH��3���������˳�ȥ���Լ�X����ΪCuO��������ͭ�ȣ������Ŀ��Ϣ��֪���Ȼ�ͭ��Һ�����������ᣬ�����Ȼ�ͭˮ�⣬������Ũ������ȴ��26��42��ᾧ�õ�CuCl2•2H2O���پ������ˡ�ϴ�ӡ�����õ������ľ��壮
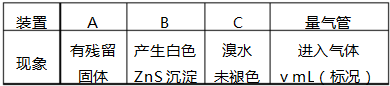
��1����Aװ���Ʊ�������Cװ�����������е�HCl��Eװ�ø���������Dװ����Cu��������Ӧ��Bװ������δ��Ӧ����������ֹ��Ⱦ������
��Ӧ���Ʊ��������ų�װ���п�������ֹͭ������������
��2�����Ȼ�ͭ���Ȼ�������Һ�лᷢ��ˮ�⣻
�ڵ���pHĿ����ʹ��Һ��������ת��ΪFe��OH��3���������˳�ȥ���Ҳ������������ʣ�
�۽����Ŀ��Ϣ��֪���Ȼ�ͭ��Һ�����������ᣬ�����Ȼ�ͭˮ�⣬������Ũ������ȴ��26��42��õ�CuCl2•2H2O���پ������ˡ�ϴ�ӡ�����õ������ľ��壻
��3���Ȼ�ͭ��N2H4��Ӧ�õ�CuCl����������Ϊ�����壬��Ϊ��������Ԫ���غ��֪����Ӧ������HCl��
����CuCl����ˮ��Ѹ��ˮ����������ͭˮ���Ӧ��ά�ַ�Ӧ��������ֹCuClˮ����������ͭˮ���
��4������CuԪ���غ����CuCl2•2H2O����������������������ʣ��ڵ�����ҺpHʱ������CuO��������ͭ���ᵼ��CuCl2•2H2O��������
��� �⣺��ͭ������ֻ��Fe����������Ӧ�õ�����������Ȼ�ͭ���Ȼ������������ܽ⣬�����Ȼ�ͭ���Ȼ���ˮ�⣬��Һ���м���X������ҺpH���õ���Һ�ң�����ϵ�в����õ�CuCl2•2H2O������Һ��ΪCuCl2��Һ�������pHĿ����ʹ��Һ��������ת��ΪFe��OH��3���������˳�ȥ���Լ�X����ΪCuO��������ͭ�ȣ������Ŀ��Ϣ��֪���Ȼ�ͭ��Һ�����������ᣬ�����Ȼ�ͭˮ�⣬������Ũ������ȴ��26��42��õ�CuCl2•2H2O���پ������ˡ�ϴ�ӡ�����õ������ľ��壮
��1����Aװ���Ʊ�������Cװ�����������е�HCl��Eװ�ø���������Dװ����Cu��������Ӧ��Bװ������δ��Ӧ����������ֹ��Ⱦ�������������������Ӹ������ӿ�˳���ǣ�a��d��e��h��i��f��g��b��
�ʴ�Ϊ��d��e��f��g��b��
��Ӧ���Ʊ��������ų�װ���п�������ֹͭ�������������ʼ��ȵ�˳��Ϊ��A��D��
�ʴ�Ϊ��A��D���ų���������ֹͭ������������
��2�����Ȼ�ͭ���Ȼ�������Һ�лᷢ��ˮ�⣬�������ܽ⣬���������Ȼ�ͭ���Ȼ���ˮ�⣬
�ʴ�Ϊ�������Ȼ�ͭ���Ȼ���ˮ�⣻
�ڵ���pHĿ����ʹ��Һ��������ת��ΪFe��OH��3���������˳�ȥ���Ҳ������������ʣ����������ơ���ˮ������ͭ���������ʣ���ѡ��c��
�۽����Ŀ��Ϣ��֪���Ȼ�ͭ��Һ�����������ᣬ�����Ȼ�ͭˮ�⣬������Ũ������ȴ��26��42��ᾧ�õ�CuCl2•2H2O���پ������ˡ�ϴ�ӡ�����õ������ľ��壬
�ʴ�Ϊ����ȴ��26��42��ᾧ�����ˣ�
��3���Ȼ�ͭ��N2H4��Ӧ�õ�CuCl����������Ϊ�����壬��Ϊ��������Ԫ���غ��֪����Ӧ������HCl����Ӧ���ӷ���ʽΪ��4Cu2++4Cl-+N2H4$\frac{\underline{\;\;��\;\;}}{\;}$4CuCl��+N2��+4H+��
����CuCl����ˮ��Ѹ��ˮ����������ͭˮ���Ӧ��ά�ַ�Ӧ��������ֹCuClˮ����������ͭˮ���
�ʴ�Ϊ��4Cu2++4Cl-+N2H4$\frac{\underline{\;\;��\;\;}}{\;}$4CuCl��+N2��+4H+����ά�ַ�Ӧ�������¶ȹ�����������ͭˮ���
��4������CuԪ���غ㣬CuCl2•2H2O��������Ϊ$\frac{100g��96%}{64g/mol}$��171g/mol=256.5g���������Ϊ$\frac{277g}{256.5g}$��100%=108%���ڵ�����ҺpHʱ������CuO��Ӧ������CuCl2��ʹ��Ʒ�������ӣ�
�ʴ�Ϊ��108%���ڵ�����ҺpHʱ������CuO��Ӧ������CuCl2��ʹ��Ʒ�������ӣ�
���� ���⿼��ʵ���Ʊ��������漰��װ�õķ������ۡ����ʵķ����ᴿ���Բ����ķ������ۡ������ⶨ�ȣ�ע�����Ŀ��Ϣ����ȡӦ�ã����ؿ���ѧ��������������������֪ʶǨ�������������Ѷ��еȣ�

 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д� �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д�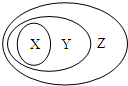 ��ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�д�����ǣ�������
��ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�д�����ǣ�������| X | Y | Z | |
| A | ����ͬϵ�� | ������ | �����廯���� |
| B | ���� | �Ͻ� | ����� |
| C | ����� | ���ӻ����� | ������ |
| D | ���������� | ���������� | ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ������ˮ��Ϻ�������Ӧ��ʹ��ˮ��ɫ | |
| B�� | �ڱ��м�������KMnO4��Һ�����ã��²�Һ��δ��ɫ | |
| C�� | 1mol������3mol H2�����ӳɷ�Ӧ��˵���ڱ����к���3��˫�� | |
| D�� | �ñ���ȴ�����������������ɫ�ľ��� |
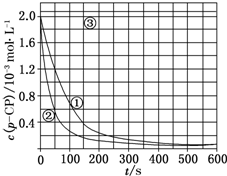 Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ��ͨ�����ڵ��ں�pH��Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�죮
Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ��ͨ�����ڵ��ں�pH��Fe2+Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p-CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�죮��ʵ����ơ�����p-CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298K��313K������ʵ���������±�����������¶Ա�ʵ�飺
��1�����������ʵ����Ʊ������в�Ҫ���ո�
| ʵ���� | ʵ��Ŀ�� | T/K | pH | c/10-3 mol•L-1 | |
| H2O2 | Fe2+ | ||||
| �� | Ϊ����ʵ�������� | 298 | 3 | 6.0 | 0.30 |
| �� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | 3 | |||
| �� | 298 | 10 | 6.0 | 0.30 | |
��2���������ͼʵ������ߣ����㽵�ⷴӦ50��150s�ڵķ�Ӧ���ʣ�v��p-CP��=8.0��10-6mol•L-1•s-1��
����������ۡ�
��3��ʵ��١��ڱ����¶����ߣ����ⷴӦ�������������о��������¶ȹ���ʱ�������½��ⷴӦ���ʼ�С�����Fenton�������Լ�H2O2�ĽǶȷ���ԭ�����������¶ȹ���ʱѸ�ٷֽ⣻
��4��ʵ��۵ó��Ľ����ǣ�pH����10ʱ����Ӧ���ܣ���ܡ����ܡ������У�
��˼���뽻����
��5��ʵ��ʱ���ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еķ�Ӧ����ֹͣ������������ͼ�е���Ϣ������һ��Ѹ��ֹͣ��Ӧ�ķ���������Һ�м������Һ��ʹ��Һ��pH���ڻ����10�����������𰸾��ɣ���
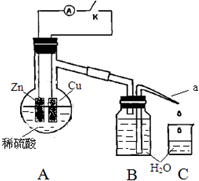 ijͬѧ����Zn��ϡH2SO4�ķ�Ӧ��
ijͬѧ����Zn��ϡH2SO4�ķ�Ӧ����1���÷�Ӧ�����ӷ���ʽ��Zn+2H+=Zn2++H2����
��2����H2ʱ����ϡ���������Ũ���ᣬԭ����ŨH2SO4����ǿ�����ԣ���������������
��3����֪��Zn��s��+$\frac{1}{2}$O2��g��=ZnO��s����H=-332kJ/mol
ZnO��s��+H2SO4��aq��=ZnSO4��aq��+H2O��l����H=-112kJ/mol
H2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-286kJ/mol
��Zn��ϡH2SO4��Ӧ����1mol H2 ʱ�ķ�Ӧ�ȡ�H=-158kJ/mol��
��4����ͬѧ������װ�ý���ʵ�飬����Ӱ�췴Ӧ���ʵ����أ�
ʵ��ʱ���ӶϿ�K��ʼ��ÿ���1���ӣ�����Ͽ���պ�K������������ÿ1 �����ڴ�a��������ˮ�������õ���ˮ�������±���ʾ��
| 1����ˮ�������Ͽ�K�� | 34 | 59 | 86 | 117 | �� | 102 |
| 1����ˮ�������պ�K�� | 58 | 81 | 112 | 139 | �� | 78 |
����ˮ����58��34��81��59��˵���ڷ�Ӧ���ڣ��պ�Kʱ�ȶϿ�Kʱ�ķ�Ӧ���ʿ죨��족������������Ҫԭ�����γ�ԭ��ط�Ӧ�ٶȿ죮
����ˮ����102��78��˵���ڷ�Ӧ���ڣ��Ͽ�Kʱ�ķ�Ӧ���ʿ��ڱպ�Kʱ�ķ�Ӧ���ʣ���Ҫԭ���ǶϿ�Kʱ����Һ�е�c��H+�����ڱպ�Kʱ��Һ�е�c��H+����
�۴�����ת����ʽ��ͬ�ĽǶȣ�����ˮ����86��81��117��112����Ҫԭ���ǶϿ�Kʱ����Ӧ�Ļ�ѧ����Ҫת�������ܣ��պ�Kʱ����Ӧ�Ļ�ѧ����Ҫת���ɵ��ܣ�ǰ��ʹ��Һ���¶����ø��ߣ��ʷ�Ӧ���ʸ��죮
���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
��ѧ��������õ���Ar��
��������ǿ����K��
����������ˮ���������ǿ�ļ���KOH��
����������ˮ����������ǿ������HClO4��
��2��DԪ�ص�����������Ӧ��ˮ����������������Һ��Ӧ�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O��
��3��A��B��C����Ԫ�ذ�ԭ�Ӱ뾶�ɴ�С��˳�����е�ΪK��Na��Mg��
��4��F���⻯��ĵ���ʽ
 ��G��H �⻯����ȶ��Եݼ���˳����HCl��HBr��
��G��H �⻯����ȶ��Եݼ���˳����HCl��HBr����5��HԪ�ظ�AԪ���γɵĻ�����Ļ�ѧʽ��NaBr��A2F2�ĵ���ʽ��
 ����
������6��B��F����Ԫ���γɵ�2��1�ͻ������������ӻ��������ӻ�������ۻ�����������õ���ʽ��ʾ���γɹ���
 ��
��