题目内容
下列反应中反应物的总能量小于生成物的总能量的是( )
| A、电解水制取H2和O2 |
| B、甲烷燃烧 |
| C、铝粉与氧化铁粉末反应 |
| D、油脂在人体内完全氧化生成CO2和H2O |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:反应物总能量高于反应物总能量,应为放热反应,常见放热反应有大多数化合反应、酸碱中和反应、金属与酸的反应,物质的燃烧等,
生成物总能量高于反应物总能量,应为吸热反应,常见吸热反应有大多数分解反应,C、CO等还原剂与金属氧化物的反应,Ba(OH)2?8H2O与NH4Cl反应等,以此解答.
生成物总能量高于反应物总能量,应为吸热反应,常见吸热反应有大多数分解反应,C、CO等还原剂与金属氧化物的反应,Ba(OH)2?8H2O与NH4Cl反应等,以此解答.
解答:
解:反应物总能量小于生成物总能量,应为吸热反应,题中B、C、D为放热反应,反应物能量高,而电解水需要电能转化为化学能,生成物总能量高,
故选:A.
故选:A.
点评:本题考查反应热与焓变,侧重于基础知识的考查,为高频考点,注意把握常见吸热反应与放热反应,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
白磷和红磷燃烧的产物都是P2O5,但是相同条件下等量的白磷和红磷燃烧前者放出热量多.以下说法正确的是( )
| A、红磷比白磷稳定 |
| B、白磷转化成红磷吸收热量 |
| C、红磷转化成白磷为放热反应 |
| D、等量的白磷和红磷相互转化时的能量变化值不相等 |
可以使湿润的红色石蕊试纸变蓝的气体是( )
| A、NO |
| B、HCl |
| C、NH3 |
| D、NO2 |
下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A、向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:NH4++H++SO42-+Ba2++2OH-═NH3?H2O+BaSO4↓+H2O | ||||
| B、酸性高锰酸钾溶液与H2O2溶液混合:2MnO4-+3H2O2+6H+═2Mn2++6H2O+O2↑ | ||||
C、用铜作电极电解饱和食盐水:2Cl-+2H2O
| ||||
D、以下有机物在碱性条件下水解的化学方程式:BrCH2-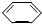 -OOCH+3NaOH -OOCH+3NaOH
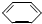 ONa+HCOONa+NaBr ONa+HCOONa+NaBr |
下列叙述:
①非金属元素的单质M能从Q的化合物中置换出非金属单质Q;
②M原子比Q原子容易得到电子;
③单质M跟H2反应比Q跟H2容易的多;
④氢化物水溶液的酸性HmM>HnQ;
⑤氧化物对应水化物的酸性HmMOx>HnQOy;
⑥熔点:M>Q;
⑦金属键M>Q.
能说明非金属元素M比非金属元素Q强的是( )
①非金属元素的单质M能从Q的化合物中置换出非金属单质Q;
②M原子比Q原子容易得到电子;
③单质M跟H2反应比Q跟H2容易的多;
④氢化物水溶液的酸性HmM>HnQ;
⑤氧化物对应水化物的酸性HmMOx>HnQOy;
⑥熔点:M>Q;
⑦金属键M>Q.
能说明非金属元素M比非金属元素Q强的是( )
| A、①②③ | B、①②③⑦ |
| C、①②③⑤⑦ | D、①②③④⑤⑦ |
鉴别Clˉ、Brˉ、Iˉ三种离子,宜选用的试剂组是( )
| A、溴水和淀粉溶液 |
| B、硝酸银溶液和稀硝酸 |
| C、氯水和四氯化碳 |
| D、氯水和碘化钾淀粉溶液 |
PbO2在酸性溶液中能将Mn2+氧化成MnO4-,本身被还原为Pb2+.取一支试管,加入适量PbO2固体和适量的稀H2SO4后滴入2mL 1mol/L MnSO4溶液.下列说法错误的是( )
| A、充分振荡后静置,溶液颜色变为紫色 |
| B、上述实验中不能用盐酸代替硫酸 |
| C、在酸性条件下,PbO2的氧化性比MnO4-的氧化性强 |
| D、若上述实验完全反应,消耗PbO2的物质的量为0.01mol |