题目内容
外界条件对盐类水解的影响(外外因)
考点:影响盐类水解程度的主要因素
专题:盐类的水解专题
分析:依据盐类水解是吸热过程,水解程度微弱,结合平衡移动原理分析影响平衡的外因.
解答:
解:盐类水解是吸热过程,外界条件对盐类水解的影响为:
①.温度:水解反应为吸热反应,升温平衡右移;
②.浓度:改变平衡体系中每一种物质的浓度,都可使平衡移动,盐的浓度越小,水解程度越大;
③.溶液的酸碱度:加入酸或碱能促进或抑制盐类的水解.例如:水解呈酸性的盐溶液,若加入碱,就会中和溶液中的H,使平衡向水解的方向移动而促进水解;若加入酸,则抑制水解;同种水解相互抑制,不同水解相互促进;
答:外界条件对盐类水解的影响①.温度:水解反应为吸热反应,升温平衡右移;
②.浓度:改变平衡体系中每一种物质的浓度,都可使平衡移动,盐的浓度越小,水解程度越大;
③.溶液的酸碱度:加入酸或碱能促进或抑制盐类的水解.例如:水解呈酸性的盐溶液,若加入碱,就会中和溶液中的H,使平衡向水解的方向移动而促进水解;若加入酸,则抑制水解;同种水解相互抑制,不同水解相互促进.
①.温度:水解反应为吸热反应,升温平衡右移;
②.浓度:改变平衡体系中每一种物质的浓度,都可使平衡移动,盐的浓度越小,水解程度越大;
③.溶液的酸碱度:加入酸或碱能促进或抑制盐类的水解.例如:水解呈酸性的盐溶液,若加入碱,就会中和溶液中的H,使平衡向水解的方向移动而促进水解;若加入酸,则抑制水解;同种水解相互抑制,不同水解相互促进;
答:外界条件对盐类水解的影响①.温度:水解反应为吸热反应,升温平衡右移;
②.浓度:改变平衡体系中每一种物质的浓度,都可使平衡移动,盐的浓度越小,水解程度越大;
③.溶液的酸碱度:加入酸或碱能促进或抑制盐类的水解.例如:水解呈酸性的盐溶液,若加入碱,就会中和溶液中的H,使平衡向水解的方向移动而促进水解;若加入酸,则抑制水解;同种水解相互抑制,不同水解相互促进.
点评:本题考查了影响盐类水解的因素分析判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列反应中反应物的总能量小于生成物的总能量的是( )
| A、电解水制取H2和O2 |
| B、甲烷燃烧 |
| C、铝粉与氧化铁粉末反应 |
| D、油脂在人体内完全氧化生成CO2和H2O |
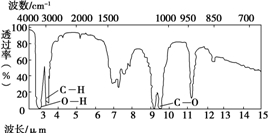 有机物A由碳、氢、氧三种元素组成.现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余).将反应生成的气体依次通过足量的浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g.回答下列问题:
有机物A由碳、氢、氧三种元素组成.现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余).将反应生成的气体依次通过足量的浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g.回答下列问题: