题目内容
【题目】某同学应用如下所示装置研究物质的性质。其中气体X的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题:
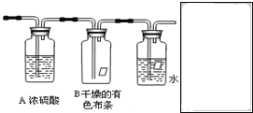
(1)B中观察到的实验现象是___。
(2)从物质性质方面来看,这样的实验设计还存在事故隐患,应如何处理,请画出装置图(填在图方框内),用化学方程式表达原理___。
【答案】有色布条不褪色  ,Cl2 +2NaOH=NaCl + NaClO + H2O
,Cl2 +2NaOH=NaCl + NaClO + H2O
【解析】
(1)干燥的氯气没有漂白性;
(2)由于氯气有毒,随意排放会造成环境污染。
(1)浓硫酸具有干燥作用,含有水蒸气的氯气通过浓硫酸后得到干燥的氯气,干燥的氯气没有漂白性,B中观察到的实验现象是干燥的有色布条不褪色;
(4)由于氯气有毒,随意排放会造成环境污染,所以该实验装置还缺少尾气处理装置。吸收氯气一般用氢氧化钠溶液,有关反应的离子方程式是Cl2 +2NaOH=NaCl + NaClO + H2O;装置图是 。
。

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案
相关题目