题目内容
下列各组离子中,一定能大量共存的是( )
| A、无色溶液中:Cu2+、Ca2+、Cl-、SO42- |
| B、强碱性溶液中:K+、Al3+、HCO3-、SO42- |
| C、pH=1的溶液中:Na+、Fe2+、NO3-、S2- |
| D、Ba2+、OH-、Cl-、K+ |
考点:离子共存问题
专题:离子反应专题
分析:A.Cu2+为蓝色;
B.强碱溶液中不能大量存在Al3+、HCO3-;
C.pH=1的溶液,显酸性,离子之间发生氧化还原反应;
D.该组离子之间不反应.
B.强碱溶液中不能大量存在Al3+、HCO3-;
C.pH=1的溶液,显酸性,离子之间发生氧化还原反应;
D.该组离子之间不反应.
解答:
解:A.Cu2+为蓝色,与无色不符,且Ca2+、SO42-结合生成沉淀不能共存,故A不选;
B.强碱溶液中不能大量存在Al3+、HCO3-,且Al3+、HCO3-相互促进水解不能共存,故B不选;
C.pH=1的溶液,显酸性,H+、Fe2+(或S2-)、NO3-离子之间发生氧化还原反应,不能共存,故C不选;
D.该组离子之间不反应,可大量共存,故D选;
故选D.
B.强碱溶液中不能大量存在Al3+、HCO3-,且Al3+、HCO3-相互促进水解不能共存,故B不选;
C.pH=1的溶液,显酸性,H+、Fe2+(或S2-)、NO3-离子之间发生氧化还原反应,不能共存,故C不选;
D.该组离子之间不反应,可大量共存,故D选;
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,涉及水解、氧化还原反应及水解反应的考查,题目难度不大.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H>0 | ||
| B、电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | ||
C、CH3COOH溶液加水稀释后,溶液中
| ||
| D、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
某有机化合物6.2g在氧气中完全燃烧,只生成8.8g CO2和5.4g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定含有氧元素 |
下列离子方程式不正确的是( )
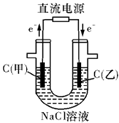
A、用铜电极电解NaCl溶液:2Cl-+2H2O
| ||||
| B、氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O | ||||
| C、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO | ||||
| D、Cl2通入FeBr2溶液中,Cl2与FeBr2物质的量之比4:5:10Fe2++6Br-+8Cl2=10Fe3++3Br2+16Cl- |
在反应:H2S+H2SO4(浓)═S+SO2+2H2O中,下列说法正确的是( )
| A、S是还原产物,SO2是氧化产物 |
| B、S是氧化产物,SO2是还原产物 |
| C、该反应的电子转移数目是6e- |
| D、H2S是还原剂,被还原为S |
用NA表示阿伏加德罗常数,下列说法中不正确的是( )
| A、在常温常压下,11.2L氯气所含的原子数目为NA |
| B、常温常压下,2.8g CO气体所含的质子数目为1.4NA |
| C、2.7g铝与足量盐酸反应转移的电子数为0.3NA |
| D、2L 0.1mol?L-1 K2SO4溶液中离子总数约为0.6NA |
下列有关物质的性质或应用的说法中正确的是( )
| A、Si是一种非金属主族元素,其氧化物可用于制作计算机芯片 |
| B、石油的催化裂化及裂解可以得到较多的轻质油和气态烯烃 |
| C、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D、蛋白质溶液中加入浓的硫酸钠溶液,有沉淀析出,这种作用称为变性 |