题目内容
下列说法不正确的是( )
| A | B | C | D |
 | 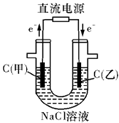 |  | 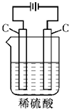 |
| 总反应的离子方程式为: 2Fe3++Cu═Cu2++2Fe2+ | 甲电极上的电极反应为: 2Cl--2e-═Cl2↑ | Pt电极上的电极反应为: O2+2H2O+4e-═4OH- | 通电一段时间后,搅拌均匀,溶液的PH值增大 |
| A、A | B、B | C、C | D、D |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.铜为负极,被氧化,正极发生还原反应,Fe3+得电子生成Fe2+;
B.由电子流向可知甲为阳极,乙为阴极;
C.为铁的吸氧腐蚀装置,铁为负极,Pt为正极;
D.电解硫酸溶液,阳极生成氧气,阴极生成氢气,溶液浓度增大.
B.由电子流向可知甲为阳极,乙为阴极;
C.为铁的吸氧腐蚀装置,铁为负极,Pt为正极;
D.电解硫酸溶液,阳极生成氧气,阴极生成氢气,溶液浓度增大.
解答:
解:A.铜为负极,被氧化,正极发生还原反应,Fe3+得电子生成Fe2+,总反应式为2Fe3++Cu═Cu2++2Fe2+,故A正确;
B.由电子流向可知甲为阳极,乙为阴极,阳极发生氧化反应,电极方程式为2Cl--2e-═Cl2↑,故B正确;
C.为铁的吸氧腐蚀装置,铁为负极,Pt为正极,正极发生还原反应,电极方程式为O2+2H2O+4e-═4OH-,故C正确;
D.电解硫酸溶液,阳极生成氧气,阴极生成氢气,溶液浓度增大,溶液pH减小,故D错误.
故选D.
B.由电子流向可知甲为阳极,乙为阴极,阳极发生氧化反应,电极方程式为2Cl--2e-═Cl2↑,故B正确;
C.为铁的吸氧腐蚀装置,铁为负极,Pt为正极,正极发生还原反应,电极方程式为O2+2H2O+4e-═4OH-,故C正确;
D.电解硫酸溶液,阳极生成氧气,阴极生成氢气,溶液浓度增大,溶液pH减小,故D错误.
故选D.
点评:本题考查较为综合,涉及原电池和电解池知识,为高考常见题型,侧重于学生的分析能力的考查,注意把握原电池和电解池的组成以及工作原理,把握电极方程式的书写,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
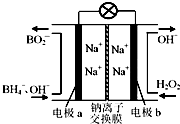 据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A、电池放电时Na+从a极区移向b极区 |
| B、每消耗3mol H2O2,转移的电子为3mol |
| C、电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D、该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |
下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是( )
A、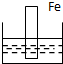 |
B、 |
C、 |
D、 |
下列各组离子中,一定能大量共存的是( )
| A、无色溶液中:Cu2+、Ca2+、Cl-、SO42- |
| B、强碱性溶液中:K+、Al3+、HCO3-、SO42- |
| C、pH=1的溶液中:Na+、Fe2+、NO3-、S2- |
| D、Ba2+、OH-、Cl-、K+ |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ?mol-1则氢气的燃烧热为△H=-241.8kJ?mol-1 |
| B、已知C(石墨,s)═C(金刚石,s);△H=+1.9kJ?mol-1,可知石墨比金刚石更稳定 |
| C、已知NaOH(ag)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.4kJ?mol-1可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.4kJ |
| D、已知2C(s)+2O2(g)═2CO2(g);△H1 2C(s)+O2(g)═2CO(g);△H2,则△H1>△H2 |
下列说法错误的是( )
| A、在水溶液里,乙酸分子中的-CH3可以电离出H+ |
| B、红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 |
| C、用金属钠可区分乙醇和乙醚 |
| D、盐析可提纯蛋白质并保持其生理活性 |
由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种或两种以上元素,它们分子中质子总数均与氩原子的质子数相同,已知甲是气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
| A、某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B、乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C、丙中含有第2周期ⅣA族的元素,则丙一定是甲烷的同系物 |
| D、丁和甲含有相同元素,且该元素在二者中的百分含量相同,则丁中一定含有-l价元素 |
下列离子在溶液中能大量共存的是( )
| A、Fe3+、NH4+、SCN-、Cl- |
| B、Fe2+、NH4+、Cl-、OH- |
| C、Al3+、Na+、OH-、Cl- |
| D、Na+、H+、NO3-、SO42- |
