题目内容
某有机化合物6.2g在氧气中完全燃烧,只生成8.8g CO2和5.4g H2O.下列说法正确的是( )
| A、该化合物仅含碳、氢两种元素 |
| B、该化合物中碳、氢原子个数比为1:4 |
| C、无法确定该化合物是否含有氧元素 |
| D、该化合物中一定含有氧元素 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据n=
计算8.8g CO2和5.4g H2O的物质的量,计算C、H原子物质的量,进而计算C、H元素的质量,根据质量守恒定律判断该化合物中是否含有氧元素,据此解答.
| m |
| M |
解答:
解:8.8g CO2的物质的量=
=0.2mol,n(C)=0.2mol,m(C)=0.2mol×12g/mol=2.4g,
5.4g H2O的物质的量=
=0.3mol,n(H)=0.6mol,m(H)=0.6mol×1g/mol=0.6g,
由于m(C)+m(H)=2.4g+0.6g=3g<6.2g,故该化合物中还含有氧元素,有机物分子中n(C):n(H)=0.2mol:0.6mol=1:3,
由上述分析可知,ABC错误,D正确,故选D.
| 8.8g |
| 44g/mol |
5.4g H2O的物质的量=
| 5.4g |
| 18g/mol |
由于m(C)+m(H)=2.4g+0.6g=3g<6.2g,故该化合物中还含有氧元素,有机物分子中n(C):n(H)=0.2mol:0.6mol=1:3,
由上述分析可知,ABC错误,D正确,故选D.
点评:本题考查有机物组成的判断,侧重质量守恒定律的运用,比较基础.

练习册系列答案
相关题目
正确的实验设计和操作是实验成功的重要因素,下列实验设计或操作正确的是( )
A、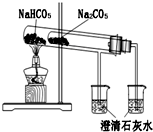 证明热稳定性Na2CO3>NaHCO3 |
B、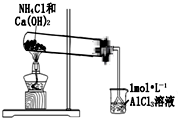 证明氢氧化铝的两性 |
C、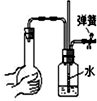 检查装置气密性 |
D、 测定KClO3元素的质量 |
下列说法不正确的是( )
| A、在一定条件下,催化分解80g SO3,混合气体中氧原子数为3×6.02×1023 |
| B、一定条件下,铁与水蒸气反应生成8.96L H2时(已折合成标况),转移的电子数为0.8×6.02×1023 |
| C、含有非极性键的数目为6.02×1023的Na2O2与水充分反应,标况下产生O2 22.4L |
| D、100mL 1mol/L AlCl3与3mol/L NaCl的混合溶液中,Cl-的个数为0.6×6.02×1023 |
下列离子方程式中正确的是( )
| A、Fe(OH)3滴加稀盐酸:OH-+H+=H2O |
| B、向石灰乳[Ca(OH)2]溶液通入过量的二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
| C、MgCl2溶液中滴加氨水:Mg2++2OH-=Mg(OH)2↓ |
| D、NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+=BaSO4↓ |
下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是( )
A、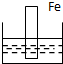 |
B、 |
C、 |
D、 |
下列关于实验操作中先后顺序的叙述错误的是( )
| A、实验室制取气体时,先装药品,再检查装置气密性 |
| B、用托盘天平称量药品时,先调节天平平衡,再称量 |
| C、实验室用CO与Fe2O3反应制取铁时,先通CO,再点燃酒精灯 |
| D、稀释浓硫酸时,先在烧杯内倒入水,再缓慢注入浓硫酸,并不断搅拌 |
下列各组离子中,一定能大量共存的是( )
| A、无色溶液中:Cu2+、Ca2+、Cl-、SO42- |
| B、强碱性溶液中:K+、Al3+、HCO3-、SO42- |
| C、pH=1的溶液中:Na+、Fe2+、NO3-、S2- |
| D、Ba2+、OH-、Cl-、K+ |
分子式为C5H11Cl的卤代烃发生消去反应生成的烯烃种数是( )
| A、3 | B、4 | C、5 | D、6 |
