题目内容
7.含下列溶质的稀溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH值增大的是( )| A. | NaOH | B. | H2SO4 | C. | AgNO3 | D. | Na2SO4 |
分析 A.电解氢氧化钠溶液,本质是电解水,氢氧化钠溶液浓度增大;
B.电解硫酸溶液,本质是电解水,硫酸的浓度增大;
C.电解AgNO3溶液,阳离子为Ag+放电,阴离子为OH-放电,反应中有HNO3生成;
D.电解Na2SO4溶液,本质是电解水,Na2SO4的浓度增大,Na2SO4属于强酸强碱盐,溶液呈中性.
解答 解:A.电解氢氧化钠溶液,本质是电解水,氢氧化钠溶液浓度增大,碱性增强,溶液pH增大,故A符合;
B.电解硫酸溶液,本质是电解水,硫酸的浓度增大,溶液酸性增强,溶液pH减小,故B不符合;
C.电解AgNO3溶液,阳离子为Ag+放电,阴离子为OH-放电,反应中有HNO3生成,溶液酸性增强,溶液pH减小,故C不符合;
D.电解Na2SO4溶液,本质是电解水,Na2SO4的浓度增大,Na2SO4属于强酸强碱盐,溶液呈中性,溶液pH不变,故D不符合,
故选A.
点评 本题考查电解原理,关键是明确离子的放电顺序判断发生的反应,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.m g Fe、Fe3O4、Fe2O3的混合物用足量H2还原,固体质量减少4.8g;若将等质量的混合物加入足量的稀硝酸中,产生2.24LNO气体(标准状况下).有关该混合物的下列说法不正确的是( )
| A. | 参加反应的H2和硝酸的物质的量之比为3:1 | |
| B. | 混合物中氧原子的物质的量为0.3mol | |
| C. | 混合物中铁原子的物质的量为0.3mol | |
| D. | 参加反应的硝酸的物质的量为1mol |
15.下列变化涉及的反应类型中,属于加成反应的是( )
| A. | 苯→环已烷 | B. | 乙烯→聚乙烯 | C. | 苯→溴苯 | D. | 甲烷→四氯甲烷 |
2.下列离子方程式书写正确的是( )
| A. | 工业上将硫酸工业尾气SO2持续通入氨水中:SO2+OH-═HSO3- | |
| B. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 用惰性电极电解KOH溶液时阴极电极反应:2H2O-4e-═O2↑+4H+ | |
| D. | NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
19.将有机物完全燃烧,生成CO2和H2O.将6g该有机物的完全燃烧产物通过浓H2SO4,浓H2SO4增重7.2g,再通过碱石灰,又增重13.2g.该有机物分子式为( )
| A. | C3H8O | B. | C2H6O | C. | C2H4O2 | D. | C4H10 |
17.下列各组中两个反应的类型相同的是( )
| A. | 苯转化为溴苯、苯酚转化为环己醇 | |
| B. | 由乙醇制溴乙烷、由乙烯制溴乙烷 | |
| C. | 乙烯使溴水褪色、乙醇使酸性重铬酸钾溶液变为蓝绿色 | |
| D. | 由乙炔制氯乙烯、由氯乙烯制聚氯乙烯 |
 A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子.
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A、D同主族,E和其它元素既不同期也不同主族,B、C、D最高价氧化物的水化物两两混合均能发生反应,A和E可组成离子化合物,其晶体结构示意图如图所示,其中“●”代表阳离子,“○”代表阴离子. H++F-.
H++F-.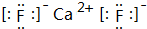 ,其晶体类型为离子晶体.
,其晶体类型为离子晶体.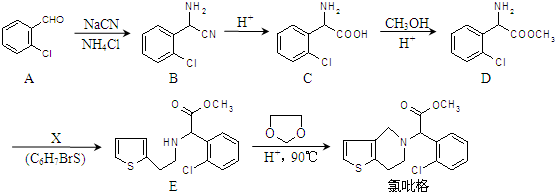
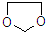 在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O
在酸性条件下生成氯吡格雷和另一种常见有机物,该有机物在浓硫酸催化下,加热脱水生成乙炔,试写出该有机物脱水生成乙炔的方程式.CH2OHCH2OH$→_{△}^{浓H_{2}SO_{4}}$CH≡CH↑+2H2O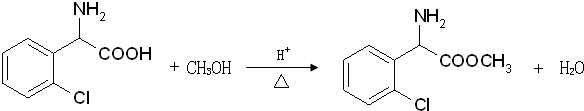
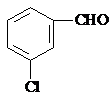 、
、 、
、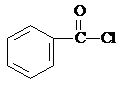 .
.