题目内容
【题目】如图是闪锌矿(主要成分是ZnS,含有少量FeS)制备ZnSO4·7H2O的一种工艺流程:闪锌矿粉→溶浸→除铁→结晶→ZnSO47H2O。已知:相关金属离子浓度为0.1mol/L时形成氢氧化物沉淀的pH范围如表:
金属离子 | Fe3+ | Fe2+ | Zn2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)闪锌矿在溶浸之前会将其粉碎,其目的是_____________。
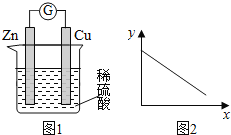
(2)溶浸过程使用过量的Fe2(SO4)3溶液和H2SO4浸取矿粉,发生的主要反应是:ZnS+2Fe3+=Zn2++2Fe2++S。
①浸出液中含有的阳离子包括Zn2+、Fe2+、_____________。
②若改用CuSO4溶液浸取,发生复分解反应,也能达到浸出锌的目的,写出离子方程式_____________。
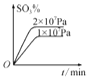
(3)工业除铁过程需要控制沉淀速率,因此分为还原和氧化两步先后进行,如图。还原过程将部分Fe3+转化为Fe2+,得到pH小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入O2。下列说法正确的是_____________(填序号)。
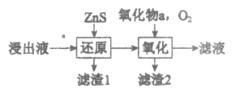
A. 氧化物a可以是ZnO
B. 滤渣2的主要成分是Fe(OH)2
C. 加入ZnS的量和通入O2的速率都可以控制溶液中的c(Fe3+)
【答案】增大表面积,提高反应速率 Fe3+、H+ ZnS+Cu2+=Zn2++CuS AC
【解析】
闪锌矿(主要成分是ZnS,含有FeS),加硫酸和Fe2(SO4)3,发生ZnS+2Fe3+=Zn2++2Fe2++S,过滤可除去S;浸出液中先加ZnS还原,分离出滤渣1为S,滤液中通入氧气可氧化亚铁离子生成铁离子,加ZnO调节pH,铁离子转化为沉淀,则滤渣2为Fe(OH)3,过滤分离出滤液经蒸发浓缩得到ZnSO47H2O,以此来解答。
(1)粉碎闪锌矿可增大接触面积,加快反应速率;
(2)①使用过量的Fe2(SO4)3溶液和H2SO4浸取矿粉,所以阳离子为Zn2+、Fe2+、Fe3+、H+;
②用CuSO4溶液浸取,发生复分解反应,根据元素守恒可知离子方程式为:ZnS+Cu2+=Zn2++CuS;
(3)A. ZnO为碱性氧化物,可增大酸性溶液pH值,同时不引入新的杂质,故A正确;
B. 根据分析可知滤渣2主要为Fe(OH)3,故B错误;
C. 加入ZnS可将铁离子还原,通入氧气可将亚铁离子氧化成铁离子,所以加入ZnS的量和通入O2的速率都可以控制溶液中的c(Fe3+),故C正确;
综上所述选AC。