题目内容
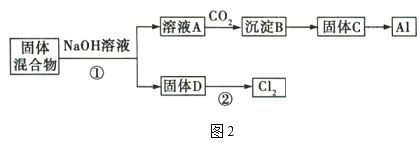
【题目】实验室里从海藻中提取碘的流程如下图:

(1)指出制取碘的过程中有关的实验操作名称(或仪器):
①操作名称________________,②仪器________________。
(2)提取碘的过程中,可供选择的有机溶剂是________(填字母序号)。
a.甲苯、酒精 b.四氯化碳、苯
c.汽油、乙酸 d.汽油、甘油
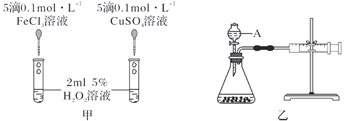
(3)含碘的有机物溶液中提取碘和回收有机溶剂,还需要经过蒸馏,观察下列实验装置指出其错误之处,并指出正确操作。____________________________________。

【答案】过滤 分液漏斗 b 烧杯不能直接加热(垫上石棉网加热),温度计伸入液面以下(温度计水银球与蒸馏烧瓶支管口相平),冷凝水上进下出(冷凝水下进上出)
【解析】
海藻灼烧得到海藻灰,浸泡得到悬浊液,过滤得到含I-离子的溶液,通入适量氯气,氧化碘离子为碘单质,加入有机萃取剂分液,得到含碘单质的有机溶液,从有机溶液中提取碘,据此分析解答。
(1)①是分离固体和液体,为过滤,②将碘水中的碘单质萃取出来,仪器为分液漏斗,故答案为:过滤;分液漏斗;
(2)萃取的基本原则是两种溶剂互不相溶,且溶质在一种萃取剂中的溶解度比在原溶剂中大的多,酒精、乙酸、甘油都会与水互溶,a、c、d项错误,可用四氯化碳或苯,b项正确,故答案为:b;
(3)根据蒸馏示意图,对烧杯加热应垫石棉网,温度计水银球应与烧瓶支管口相平,冷凝水应是下进上出,故答案为:烧杯不能直接加热(垫上石棉网加热),温度计伸入液面以下(温度计水银球与蒸馏烧瓶支管口相平),冷凝水上进下出(冷凝水下进上出)。

【题目】如图是闪锌矿(主要成分是ZnS,含有少量FeS)制备ZnSO4·7H2O的一种工艺流程:闪锌矿粉→溶浸→除铁→结晶→ZnSO47H2O。已知:相关金属离子浓度为0.1mol/L时形成氢氧化物沉淀的pH范围如表:
金属离子 | Fe3+ | Fe2+ | Zn2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)闪锌矿在溶浸之前会将其粉碎,其目的是_____________。
(2)溶浸过程使用过量的Fe2(SO4)3溶液和H2SO4浸取矿粉,发生的主要反应是:ZnS+2Fe3+=Zn2++2Fe2++S。
①浸出液中含有的阳离子包括Zn2+、Fe2+、_____________。
②若改用CuSO4溶液浸取,发生复分解反应,也能达到浸出锌的目的,写出离子方程式_____________。
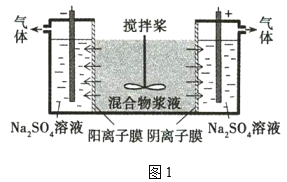
(3)工业除铁过程需要控制沉淀速率,因此分为还原和氧化两步先后进行,如图。还原过程将部分Fe3+转化为Fe2+,得到pH小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入O2。下列说法正确的是_____________(填序号)。
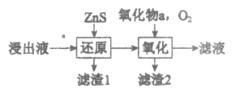
A. 氧化物a可以是ZnO
B. 滤渣2的主要成分是Fe(OH)2
C. 加入ZnS的量和通入O2的速率都可以控制溶液中的c(Fe3+)