题目内容
【题目】研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列有关判断中正确的是( )
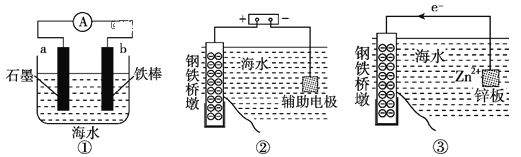
A.用装置①模拟研究时未见a上有气泡,说明铁没有被腐蚀
B.②中桥墩与外加电源正极连接能确保桥墩不被腐蚀
C.③中采用了牺牲阳极的阴极保护法保护桥墩
D.①②③中海水均是实现化学能与电能相互转化的电解质
【答案】C
【解析】
A、装置①模拟的是铁的吸氧腐蚀,在该过程中不会有气泡生成,因此不能说明铁没有被腐蚀,A错误;
B、装置②中,钢铁桥墩应该作阴极,即与电源的负极相连,才能确保桥墩不被腐蚀,B错误;
C、装置③采用了牺牲阳极的阴极保护法保护桥墩,其中阳极的金属要比铁的性质活泼,才能确保钢铁桥墩作正极,不被腐蚀,C正确;
D、海水是混合物,电解质是化合物,D错误;
故选C。

练习册系列答案
相关题目
【题目】某温度下, 反应H2(g)+CO2(g)![]() H2O(g)+CO(g)的平衡常数
H2O(g)+CO(g)的平衡常数![]() 。该温度下在体积均为10 L的三个密闭容器中分别加入反应物,起始加入量如图所示:下列判断不正确的是
。该温度下在体积均为10 L的三个密闭容器中分别加入反应物,起始加入量如图所示:下列判断不正确的是
起始量 | 甲 | 乙 | 丙 |
H2 (mol) | 1 | 2 | 2 |
CO2(mol) | 1 | 1 | 2 |
A.反应开始时,甲中的反应速率最慢,丙中的反应速率最快
B.平衡时,甲和丙中CO2的转化率相等,均是60%
C.平衡时,乙中H2的转化率大于60%
D.平衡时,丙中c(H2 ) 是0. 08 mol·L-1