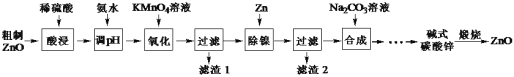
��Ŀ����
����Ŀ�����ǻ������ᶡ�����׳��Ჴ���������������������Խ�ĸ��ù���к�ǿ���������ã���ҵ�ϳ��ö��ǻ��������붡����Ũ������½���������Ӧ���Ƶã�������ij�����鿪���Ĵ����ۡ��õĻ���ԭ�ϳ����Ʊ����ǻ������ᶡ���ĺϳ�·�ߣ�
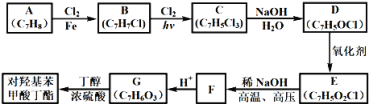
��֪������Ϣ��
��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ�����D����������Һ��Ӧ������������F�ĺ˴Ź������ױ����������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ1�s1��
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ________��
��2����B����C�Ļ�ѧ��Ӧ����ʽΪ_______���÷�Ӧ������Ϊ_______��
��3��D�Ľṹ��ʽΪ________��
��4��F�ķ���ʽΪ_______��
��5��G�Ľṹ��ʽΪ________��
��6��E��ͬ���칹���к��б������ܷ���������Ӧ�Ĺ���_______�֣����к˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2�s2�s1����______��д�ṹ��ʽ����
���𰸡��ױ� ![]() +2Cl2
+2Cl2![]()
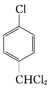 +2HCl ȡ����Ӧ
+2HCl ȡ����Ӧ ![]() C7H4O3Na2
C7H4O3Na2 ![]() 13
13 ![]()
��������
��A�ķ���ʽΪC7H8����ϵ��ת���õ�G��G�붡�����պϳɶ��ǻ������ᶡ����֪����AΪ�ױ�![]() ��GΪ
��GΪ![]() ���ױ����������������£���������λ�ϵ�Hԭ������������ȡ����Ӧ����B��BΪ
���ױ����������������£���������λ�ϵ�Hԭ������������ȡ����Ӧ����B��BΪ![]() �������Ϣ�ڿ�֪��D�к���ȩ����B�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����C��CΪ
�������Ϣ�ڿ�֪��D�к���ȩ����B�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����C��CΪ![]() ��C����������ˮ��Һ�У����ϵ���ԭ�ӷ���ȡ����Ӧ����D�������Ϣ�ٿ�֪��DΪ
��C����������ˮ��Һ�У����ϵ���ԭ�ӷ���ȡ����Ӧ����D�������Ϣ�ٿ�֪��DΪ![]() ��D�ڴ���������ȩ������������E��EΪ
��D�ڴ���������ȩ������������E��EΪ![]() ��E�ڼ��Ը��¸�ѹ������ת��ΪF��F�ữ�õ�G�������ϵ�Clԭ�ӱ�ȡ������F��ͬʱ�����кͷ�Ӧ����FΪ
��E�ڼ��Ը��¸�ѹ������ת��ΪF��F�ữ�õ�G�������ϵ�Clԭ�ӱ�ȡ������F��ͬʱ�����кͷ�Ӧ����FΪ![]() ��GΪ
��GΪ![]() ���ݴ˽��
���ݴ˽��
��������������֪AΪ![]() ��BΪ
��BΪ![]() ��CΪ
��CΪ![]() ��DΪ
��DΪ![]() ��EΪ
��EΪ![]() ��FΪ
��FΪ![]() ��
��
(1)��������������֪AΪ![]() ����A�Ļ�ѧ����Ϊ�ױ���
����A�Ļ�ѧ����Ϊ�ױ���
(2)BΪ![]() ��CΪ
��CΪ![]() ����B��Cl2�ڹ���ʱ�������ϵ�ȡ����Ӧ����C���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ
����B��Cl2�ڹ���ʱ�������ϵ�ȡ����Ӧ����C���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ![]() +2Cl2
+2Cl2![]()
![]() +2HCl����Ӧ������Ϊȡ����Ӧ��
+2HCl����Ӧ������Ϊȡ����Ӧ��
(3)D�Ľṹ��ʽΪ![]() ��
��
(4) F�ṹ��ʽΪ![]() ���������ʵĽṹ��֪F�ķ���ʽΪC7H4O3Na2��
���������ʵĽṹ��֪F�ķ���ʽΪC7H4O3Na2��
(5)G�Ľṹ��ʽΪ![]() ��
��
(6)E�ṹ��ʽΪ��![]() ��E��ͬ���칹���к��б������ܷ���������Ӧ��˵�����ܺ���ȩ��������Ϊ-OOCH��-Cl�������������ڱ�����λ������λ����λ����λ����λ�ã���3�ֲ�ͬ�ṹ��Ҳ�����Dz�������-Cl��-OH��-CHO���ֹ����ţ���-OH��-CHO������λʱ��-Cl��4�ֲ�ͬλ�ã���-CHO��-OH���ڼ�λʱ��-Cl��4�ֲ�ͬλ�ã���-OH��-CHO���ڶ�λʱ��-Cl��2�ֲ�ͬλ�ã��ʿ��ܵ�ͬ���칹������Ϊ3+4+4+2=13�֣����к˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2��2��1����
��E��ͬ���칹���к��б������ܷ���������Ӧ��˵�����ܺ���ȩ��������Ϊ-OOCH��-Cl�������������ڱ�����λ������λ����λ����λ����λ�ã���3�ֲ�ͬ�ṹ��Ҳ�����Dz�������-Cl��-OH��-CHO���ֹ����ţ���-OH��-CHO������λʱ��-Cl��4�ֲ�ͬλ�ã���-CHO��-OH���ڼ�λʱ��-Cl��4�ֲ�ͬλ�ã���-OH��-CHO���ڶ�λʱ��-Cl��2�ֲ�ͬλ�ã��ʿ��ܵ�ͬ���칹������Ϊ3+4+4+2=13�֣����к˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2��2��1����![]() ��
��