题目内容
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 0.1 mol组成为C2H6O的有机物,所含C-H键数目可能为0.5NA | |
| B. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| C. | 0.1 mol N2与0.3 mol H2在密闭容器中,在催化剂作用下充分反应,生成氨分子数为0.2NA | |
| D. | 标准状况下,22.4 L HF所含的分子数目为NA |
分析 A、C2H6O可能为二甲醚,有可能为乙醇,其结构不能确定,则含有的碳氢键不能确定;
B、从随反应进行盐酸浓度减小到一定程度,不再和二氧化锰反应生成氯气分析;
C、合成氨的反应为可逆反应,反应物只能部分转化成生成物;
D、标况下,HF为液态.
解答 解:A、该有机物若为二甲醚,则0.1mol中含有0.6mol碳氢键,若为乙醇,则含有0.5mol碳氢键,故所含C-H键数目可能为0.5NA,故A正确;
B、8.7g MnO2物质的量为0.1mol,40mL10mol/L的浓盐酸物质的量为4mol,按照化学方程式中的反应比应恰好反应,但浓盐酸在反应过程中浓度逐渐减小,当为稀盐酸时不再和二氧化锰反应生成氯气,所以生成的氯气分子数小于0.1NA,故B错误;
C、该反应为可逆反应,生成的氨气的物质的量小于0.2mol,NH3分子数小于0.2NA,故C错误;
D、标况下,HF为液态,不能根据气体摩尔体积来计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断正确的是( )
| A. | 原子晶体干冰的熔点、沸点与干冰的相同 | |
| B. | 原子晶体干冰易气化,可用作制冷材料 | |
| C. | 原子晶体干冰硬度大,可用作耐磨材料 | |
| D. | 每摩尔原子晶体干冰中含2mol C-O键 |
3.下列离子方程式中,不正确的是( )
| A. | 向Al2(SO4)3溶液中滴入过量氨水:Al3++4NH3•H2O=AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 向NaOH溶液中通入Cl2:2OH-+Cl2=Cl-+ClO-+H2O | |
| C. | 向CaCO3中加入稀盐酸:CaCO3+2H+=Ca2++CO2↑+H2O | |
| D. | 向FeBr2溶液中通入少量的Cl2:2Fe2++Cl2=2Fe3++2Cl- |
20.下列物质属于离子化合物的是( )
| A. | SiO2 | B. | CCl4 | C. | NaCl | D. | H2O |
4.下列反应中,硝酸只体现氧化性的是( )
| A. | CuO+HNO3 | B. | Cu+HNO3 | C. | FeO+HNO3 | D. | C+HNO3(浓) |
1.下列事实不能用有机物分子内基团间的相互影响解释的是( )
| A. | 甲苯能使KMnO4酸性溶液褪色而苯和甲烷不能 | |
| B. | 苯酚能跟NaOH溶液反应而乙醇不能 | |
| C. | 乙烯能发生加成反应而乙烷不能 | |
| D. | 苯在50:60℃时发生硝化反应而甲苯在30℃时即可发生硝化反应 |
2.某气体由烯烃和炔烃混合而成,经测定其密度为同条件下H2的13.5倍,则下列说法中正确的是( )
| A. | 混合气体中一定有乙烯 | B. | 混合气体中一定有乙炔 | ||
| C. | 混合气体可能由丙炔和丙烯组成 | D. | 混合气体一定由乙烯和乙炔组成 |
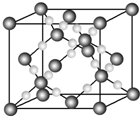 A、B、C、D、E、F为原子序数依次增大的短周期主族元素.A、C、D可形成常见的气态单质,A、E最外层电子数与其电子层数相等.B、F同主族,B元素基态原子核外电子平均分布在3个不同的能级上.C元素原子的最高能级上有3个未成对电子.F的一种单质与FD2晶体类型相同.
A、B、C、D、E、F为原子序数依次增大的短周期主族元素.A、C、D可形成常见的气态单质,A、E最外层电子数与其电子层数相等.B、F同主族,B元素基态原子核外电子平均分布在3个不同的能级上.C元素原子的最高能级上有3个未成对电子.F的一种单质与FD2晶体类型相同.