题目内容
2.1999年美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰,下列推断正确的是( )| A. | 原子晶体干冰的熔点、沸点与干冰的相同 | |
| B. | 原子晶体干冰易气化,可用作制冷材料 | |
| C. | 原子晶体干冰硬度大,可用作耐磨材料 | |
| D. | 每摩尔原子晶体干冰中含2mol C-O键 |
分析 A.原子晶体具有很高的熔沸点很高,分子晶体的熔沸点较低;
B.原子晶体沸点很高;
C.原子晶体硬度大,可用作耐磨材料;
D.二氧化碳中,1个C原子形成4个C-O键.
解答 解:A.原子晶体具有很高的熔点、沸点、硬度大,分子晶体的熔点较低,干冰属于分子晶体,则原子晶体干冰的熔点、沸点与干冰的不同,故A错误;
B.原子晶体干冰有很高的沸点,不易汽化,不可用作致冷剂,故B错误;
C.原子晶体硬度大,所以原子晶体干冰的硬度大,可用作耐磨材料,故C正确;
D.二氧化碳中,1个C原子形成4个C-O键,故1mol原子晶体干冰中含4molC-O键,故D错误,
故选C.
点评 本题以信息为载体,考查原子晶体的性质与结构,注意基础知识的掌握,难度中等.

练习册系列答案
相关题目
12.给烷烃 命名时,应该认定主链上的碳原子数是( )
命名时,应该认定主链上的碳原子数是( )
 命名时,应该认定主链上的碳原子数是( )
命名时,应该认定主链上的碳原子数是( )| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
13.物质的量相等的下列烃,在相同条件下完全燃烧,耗氧量最多的是( )
| A. | C2H6 | B. | C3H6 | C. | C4H6 | D. | C7H16 |
10.将物质的量比为1:4的甲烷和氯气混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是( )
| A. | CH3CH | B. | CH2Cl2 | C. | CCl4 | D. | HCl |
17.下面的能级表示中正确的是( )
| A. | 1p | B. | 2d | C. | 3f | D. | 4s |
7.有关化学键的叙述不正确的是( )
| A. | 卤素与碱金属容易形成离子键 | |
| B. | CH4分子中只有共价键 | |
| C. | 碳元素一般容易生成含共价键的共价化合物 | |
| D. | 在NaOH中只有离子键 |
11. 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br- 2Fe3++2I-═2Fe2++I2,则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br- 2Fe3++2I-═2Fe2++I2,则下列有关说法中,不正确的是( )
 向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br- 2Fe3++2I-═2Fe2++I2,则下列有关说法中,不正确的是( )
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br- 2Fe3++2I-═2Fe2++I2,则下列有关说法中,不正确的是( )| A. | 还原性:I->Fe2+>Br- | |
| B. | 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| C. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 | |
| D. | 原混合溶液中FeBr2的物质的量为2mol |
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1 mol组成为C2H6O的有机物,所含C-H键数目可能为0.5NA | |
| B. | 8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| C. | 0.1 mol N2与0.3 mol H2在密闭容器中,在催化剂作用下充分反应,生成氨分子数为0.2NA | |
| D. | 标准状况下,22.4 L HF所含的分子数目为NA |
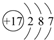 .
. .
.